Samenvatting
Achtergrond
Het syndroom van Lemierre is een zeldzaam ziektebeeld met verschillende klinische en microbiologische criteria. Het betreft vaak gezonde adolescenten die zich bij verschillende specialisten presenteren met veelvoorkomende en meestal onschuldige klachten, zoals koorts en keelpijn. Onbehandeld kent het syndroom een hoge mortaliteit.
Casus
Wij zagen een 19-jarige man op de SEH met een septische shock, nadat hij een aantal dagen koorts en keelpijn had gehad. Bij aanvullend onderzoek was er sprake van een tromboflebitis van de V. jugularis met multipele longabcessen op basis van Fusobacterium necrophorum, passend bij het syndroom van Lemierre. De patiënt werd tijdelijk opgenomen op de intensive care en is na behandeling met antibiotica en therapeutische antistolling volledig hersteld.
Conclusie
Bij patiënten met koorts en keelpijn dient het syndroom van Lemierre overwogen te worden, een zeldzame aandoening die de laatste tientallen jaren in frequentie toeneemt. Vroegtijdige herkenning is van groot belang om complicaties en mortaliteit te reduceren.
Kernpunten
- Bij jongvolwassen patiënten die zich presenteren met koorts, (doorgemaakte) keelpijn of een al dan niet pijnlijke zwelling in de hals moet altijd gedacht worden aan het syndroom van Lemierre.
- Het syndroom van Lemierre kent verschillende klinische en microbiologische criteria, waarbij een trombose van de V. jugularis geen vereiste is voor het stellen van de diagnose.
- Vanwege het snel progressieve beloop en de kans op complicaties is tijdige herkenning van dit ziektebeeld essentieel.
artikel
Het syndroom van Lemierre is een zeldzame aandoening die begint met veelvoorkomende klachten van koorts en keelpijn, meestal bij jonge en voorheen gezonde patiënten. Verschillende specialisten in de eerste en tweede lijn kunnen met dit syndroom in aanraking komen. In deze casus beschrijven we een klassieke presentatie en daarna bespreken we het syndroom in bredere zin.
Ziektegeschiedenis
Patiënt, een 19-jarige man met een blanco voorgeschiedenis, kwam bij de huisarts vanwege spierpijn, keelpijn, hoesten en kortademigheid. De huisarts zag een matig zieke man met koorts en tachycardie. Omdat de huisarts een virale luchtweginfectie vermoedde, kreeg de patiënt het advies om paracetamol te nemen en bij verslechtering contact op te nemen. De klachten waren 8 dagen later toegenomen met persisterende koorts, nachtzweten, keelpijn met globusgevoel en braken. Hij had pijn links in de hals en thoracale pijn bij doorzuchten. Op verdenking van een longembolie dan wel een pneumonie werd de patiënt naar de SEH verwezen.
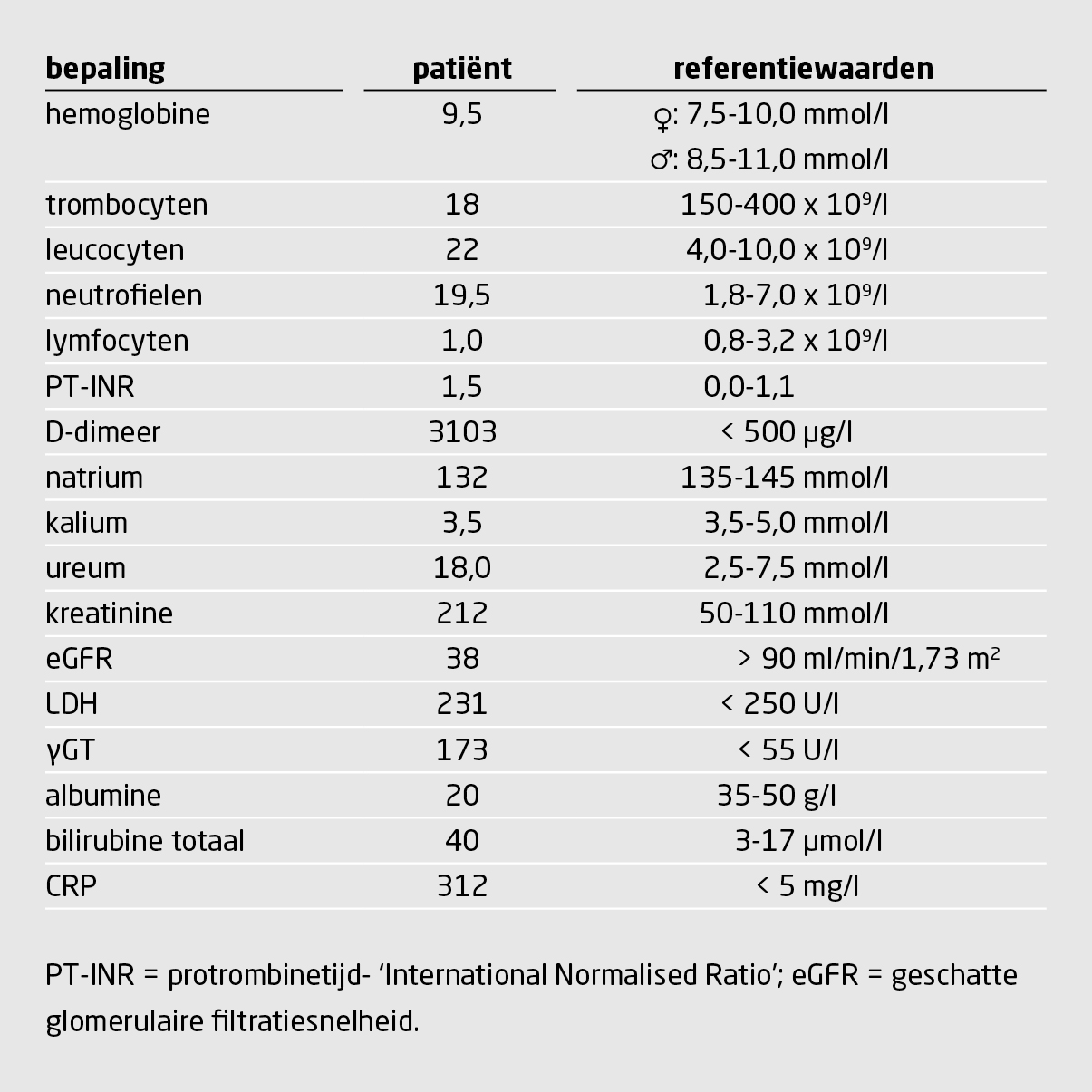
Op de SEH zagen wij een zieke, somnolente en tachypnoïsche patiënt. De bloeddruk was 100/46 mm Hg, de hartfrequentie 120 slagen/min en de temperatuur 36,5 ℃. Inspectie van de mond- en keelholte was niet mogelijk vanwege een trismus. Bij palpatie was er sprake van pijnlijke lymfadenopathie links in de hals. Bij longauscultatie hoorden wij rechts basaal verminderd ademgeruis en links diffuus rhonchi. Laboratoriumonderzoek liet hoge waarden van de inflammatieparameters zien; de laboratoriumuitslagen wezen verder op acute nierinsufficiëntie, cholestatische leverstoornissen en diffuus intravasale stolling (tabel).
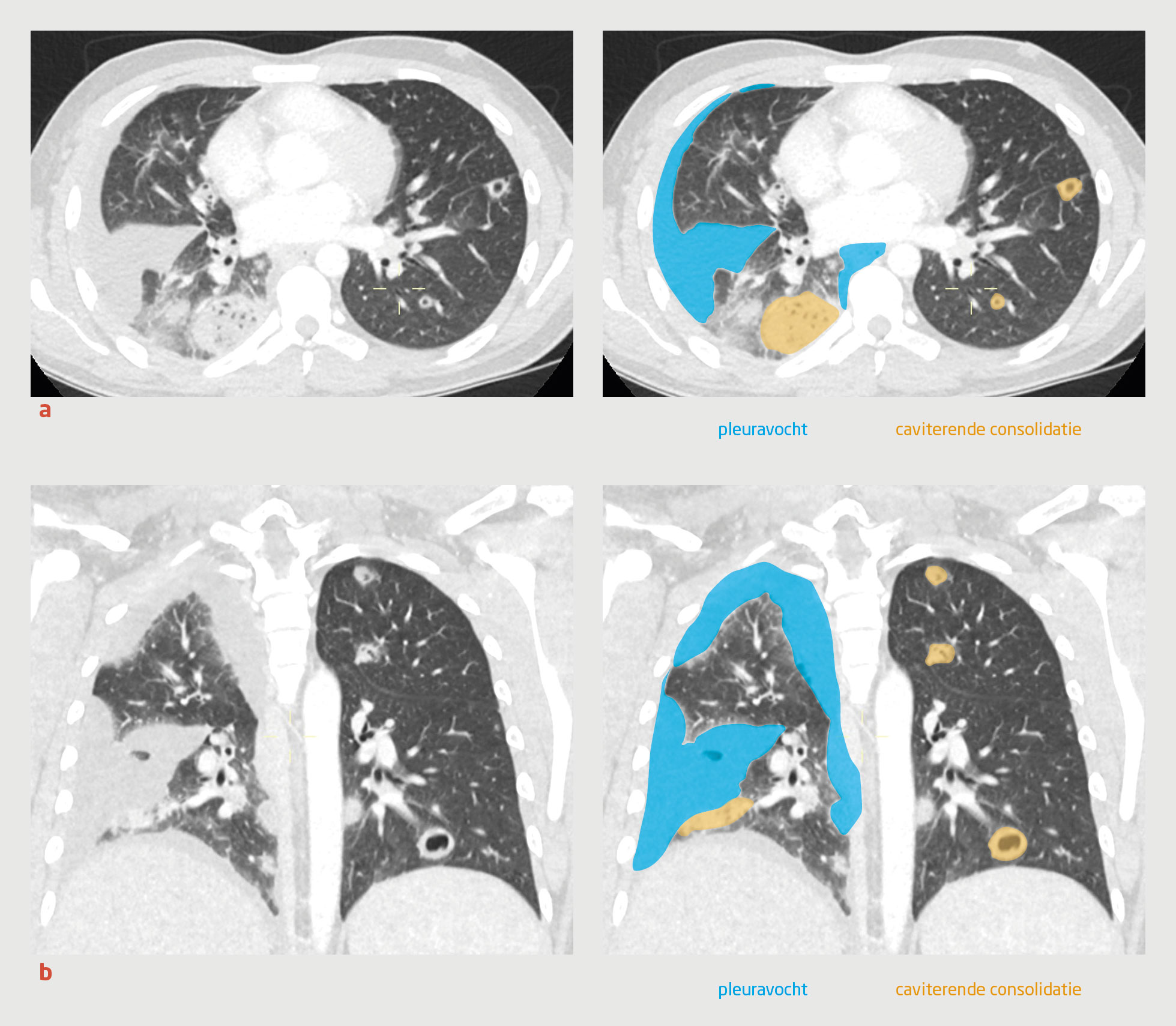
Met een brede differentiaaldiagnose van pneumosepsis, epiglottitis met peritonsillair abces, longembolie en lymfoom, lieten wij een CT van hals, thorax en abdomen verrichten. De CT-scan liet multipele, deels caviterende intrapulmonale consolidaties zien, verdacht voor septische embolieën. Echografie van de hals toonde een trombose van de V. jugularis sinistra aan (figuur).
De patiënt werd vervolgens met een septische shock op de intensive care opgenomen en behandeld met piperacilline/tazobactam en clindamycine intraveneus. Nadat de bloedkweken positief bleken te zijn voor Parvimonas micra en Fusobacterium necrophorum stapten wij over op benzylpenicilline. Na 19 dagen werd hij ontslagen met apixaban en amoxicilline per os. Bij een poliklinische controle waren de pulmonale afwijkingen nagenoeg verdwenen en liet een controle-echo een V. jugularis zonder trombose zien.
Beschouwing
Koorts en keelpijn
Koorts en keelpijn zijn meestal symptomen van een onschuldige bovensteluchtweginfectie, zoals een faryngitis of tonsillitis. Men dient alert te zijn op alarmsymptomen, zoals kwijlen, dysfagie, stridor, dyspneu, trismus en een pijnlijke zwelling in de hals. Dit kan passen bij een bovensteluchtwegobstructie of de aanwezigheid van septische embolieën. Met name wanneer bij adolescenten of jongvolwassenen sprake is van dysfagie, trismus, nekpijn of respiratoire klachten, zoals dyspneu of thoracale pijn, moet het syndroom van Lemierre overwogen worden. Daarnaast is het essentieel om bij patiënten in het ziekenhuis met koorts bloedkweken af te nemen voordat zij antibiotica toegediend krijgen.
Syndroom van Lemierre: historie en definitie
De Parijse arts Lemierre beschreef in 1936 het ziektebeeld postangineuze sepsis, ook wel necrobacillose genoemd.1 Sindsdien gebruiken auteurs verschillende klinische en microbiologische criteria voor het syndroom van Lemierre. De klassieke presentatie betreft een postangineuze sepsis met een tromboflebitis van de V. jugularis, F. necrophorum in de bloedkweek en metastatische longabcessen. Andere metastatische foci – zoals een empyeem, septische artritis of wekedelenabcessen – komen minder vaak voor.2
Er is consensus over de orofarynx als primaire infectiebron, maar er is geen eenduidige consensus over de aanwezigheid van een tromboflebitis van de V. jugularis als kenmerk; deze laatste afwijking wordt gerapporteerd bij 26-45% van de patiënten.3 Sommige artsen accepteren septische embolieën als surrogaatmarker voor tromboflebitis Zo hadden wij recentelijk een patiënte met een tonsillitis, multipele longabcessen en een bacteriëmie met F. necrophorum zonder tromboflebitis van de V. jugularis. De isolatie van F. necrophorum is overigens geen conditio sine qua non voor het syndroom van Lemierre. Uit reviews blijkt dat F. necrophorum veruit de meest voorkomende verwekker is (tot 89%), maar ook andere verwekkers zijn beschreven.3,4
Epidemiologie
Het syndroom van Lemierre werd eerder in dit tijdschrift de ‘vergeten ziekte’ genoemd.4,5 Door met name het veelvuldig penicillinegebruik in de jaren 60 en 70 werd het syndroom in die tijd weinig gerapporteerd.2,6 In het pre-antibiotische tijdperk lag de incidentie en mortaliteit veel hoger (tot 90%).1,4 Sinds 1980 wordt er een restrictiever antibioticabeleid bij bovensteluchtwegklachten gevoerd en heeft het syndroom van Lemierre zijn rentree gemaakt.
Het onderscheid tussen een bacterie of virus als verwekker is lastig. Een CRP-sneltest in de huisartsenpraktijk kan helpen om zowel onnodig antibioticagebruik te voorkomen als juist tijdig te beginnen met antibiotica, afhankelijk van de hoogte van de CRP-waarde. Naast het restrictievere antibioticabeleid zou ook de afname in tonsillectomieën een rol kunnen spelen bij de terugkeer van het syndroom.7 De jaarlijkse incidentie blijft echter laag, met 3,6 tot 14,4 patiënten per miljoen mensen.8 De mortaliteit is sterk afgenomen en is circa 5% (0-18%).9,10 Gezonde tieners en jongvolwassenen zijn het vaakst aangedaan,2,4,6,9 maar er zijn ook oudere patiënten met dit syndroom beschreven.2,6
Pathogenese en behandeling
F. necrophorum, een anaerobe gramnegatieve staaf, behoort tot de commensale orofaryngeale flora. Deze bacterie dringt door de mucosa heen, door de productie van endotoxines, en veroorzaakt zo een fulminante sepsis. De ontwikkeling van een peritonsillair abces, tromboflebitis van de tonsillaire venen en directe verspreiding in de diepe weke delen van de farynx kunnen leiden tot een tromboflebitis van de V. jugularis. F. Necrophorum heeft een trombogene werking, wat kan leiden tot intravasculaire stolling.2,10 Door hematogene verspreiding ontstaan metastatische foci in de longen, gewrichten, wekedelen, hersenen, lever en milt.1,4,11
De antibiotische behandeling bestaat in eerste instantie uit intraveneus penicilline gecombineerd met metronidazol of monotherapie met clindamycine, vanwege de kans op penicillineresistentie.2,11 Daarnaast moet er zo nodig drainage plaatsvinden van een peritonsillair abces of abcederende strooihaarden.10 Op basis van het antibiogram wordt overgestapt op smalspectrumantibiotica en op basis van het klinisch beeld – zoals koortsbeloop en adequate drainage van abcessen – kan worden besloten om over te gaan op orale therapie.2,10,11 Een behandelduur van 4-6 weken lijkt de beste uitkomsten te geven.10,11 Er bestaat converse in de literatuur over de behandeling met anticoagulantia bij een tromboflebitis, maar adequate studies hiernaar ontbreken.2,12
Terugblik op de patiënt
Onze patiënt was bij het bezoek aan de huisarts matig ziek en had keelpijn, koorts en een tachycardie. Een beoordeling van het KNO-gebied, een herbeoordeling op korte termijn en een CRP-sneltest hadden wellicht complicaties kunnen voorkomen. Wij adviseren om bij jonge patiënten met koorts en keelpijn het syndroom van Lemierre te overwegen en laagdrempelig bloedkweken af te nemen.
Conclusie
Het syndroom van Lemierre is zeldzaam. Het treft veelal jonge patiënten die zich presenteren met koorts en keelpijn. Tijdige herkenning en behandeling van dit potentieel fatale syndroom is essentieel.
Literatuur
-
Lemierre A. On certain septicaemias due to anaerobic organisms. Lancet. 1936;227:701-3. doi:10.1016/S0140-6736(00)57035-4.
-
Riordan T, Wilson M. Lemierre’s syndrome: more than a historical curiosa. Postgrad Med J. 2004;80:328-34. doi:10.1136/pgmj.2003.014274. Medline
-
Riordan T. Human infection with Fusobacterium necrophorum (Necrobacillosis), with a focus on Lemierre’s syndrome. Clin Microbiol Rev. 2007;20:622-59. doi:10.1128/CMR.00011-07. Medline
-
Blok WL, Meis JFGM, Gyssens IC, Gimbrère JSF, Horrevorts AM. Postangineuze sepsis door Fusobacterium necrophorum: het syndroom van Lemierre. Ned Tijdschr Geneeskd. 1993;137:1013-6.
-
Fleskens AJHM, Scheltinga MRM, Van Eerten PV, Verhoef LHM, Pasmans HLM, Vreugdenhil G. Keelpijn en een gezwollen hals: syndroom van Lemierre totdat het tegendeel is bewezen. Ned Tijdschr Geneeskd. 2006;150:2461-6.
-
Brazier JS, Hall V, Yusuf E, Duerden BI. Fusobacterium necrophorum infections in England and Wales 1990-2000. J Med Microbiol. 2002;51:269-72. doi:10.1099/0022-1317-51-3-269. Medline
-
Kuppalli K, Livorsi D, Talati NJ, Osborn M. Lemierre’s syndrome due to Fusobacterium necrophorum. Lancet Infect Dis. 2012;12:808-15. doi:10.1016/S1473-3099(12)70089-0. Medline
-
Hagelskjaer Kristensen L, Prag J. Lemierre’s syndrome and other disseminated Fusobacterium necrophorum infections in Denmark: a prospective epidemiological and clinical survey. Eur J Clin Microbiol Infect Dis. 2008;27:779-89. doi:10.1007/s10096-008-0496-4. Medline
-
Chirinos JA, Lichtstein DM, Garcia J, Tamariz LJ. The evolution of Lemierre syndrome: report of 2 cases and review of the literature. Medicine (Baltimore). 2002;81:458-65. doi:10.1097/00005792-200211000-00006. Medline
-
Van der Woerd WL, Veldhoen ES, Avis WA. Een ernstige Fusobacterium-infectie: het syndroom van Lemierre. Tijdschrift voor Infectieziekten. 2008;3:28-33.
-
Nadkarni MD, Verchick J, O’Neill JC. Lemierre syndrome. J Emerg Med. 2005;28:297-9. doi:10.1016/j.jemermed.2004.09.011. Medline
-
Eilbert W, Singla N. Lemierre’s syndrome. Int J Emerg Med. 2013;6:40. doi:10.1186/1865-1380-6-40. Medline



Reacties