Samenvatting
PSMA-PET-CT is een diagnostische techniek voor patiënten met prostaatkanker. Het maakt gebruik van een radioligand dat specifiek bindt aan het prostaat-specifiek membraanantigeen (PSMA), dat tot expressie komt in prostaatkankercellen. PSMA-PET-CT is zeer effectief gebleken bij de prostaatkankerdiagnostiek, zowel bij primaire stadiëring als bij re-stadiëring. PSMA-PET-CT heeft een veel grotere gevoeligheid voor de detectie van metastasen dan de traditionele CT en skeletscintigrafie, waardoor metastasen in een veel vroegere fase gedetecteerd kunnen worden. De klinische relevantie van de betere detectie wordt nu volop onderzocht. Stadiëring met PSMA-PET-CT leidt er soms toe dat van operaties wordt afgezien doordat afstandsmetastasen worden gevonden die niet met conventioneel beeldvormend onderzoek gedetecteerd waren. In Nederland is PSMA-PET-CT tegenwoordig geïndiceerd voor zowel de detectie van metastasen bij primaire prostaatkankerdiagnostiek als voor prostaatkankerdetectie bij patiënten met een biochemisch recidief van de ziekte.
artikel
Welke techniek?
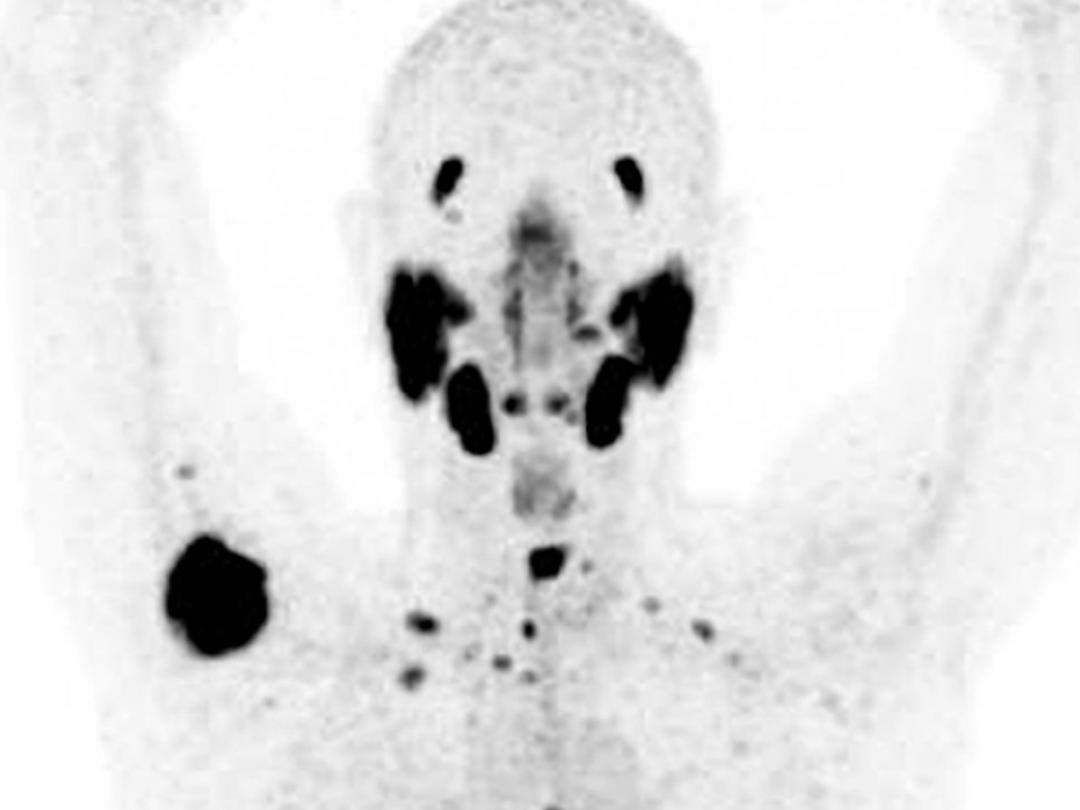
PSMA-PET-CT is een diagnostische techniek voor patiënten met prostaatkanker.1 Het maakt gebruik van een radioligand dat specifiek bindt aan het prostaat-specifiek membraanantigeen (PSMA), dat tot expressie komt in prostaatkankercellen. Hoe agressiever de prostaatkanker, hoe meer PSMA tot expressie komt. De verdeling van het radioligand in het lichaam wordt in beeld gebracht met de PET-scanner. De informatie over lokalisaties van prostaatkanker volgens de PSMA-PET-scan wordt gecombineerd met de anatomische informatie van de CT-scan (figuur).

Wat is er inmiddels bekend over de effectiviteit?
Internationaal is er in korte tijd veel onderzoek gedaan naar PSMA-PET-CT. Deze techniek is zeer effectief gebleken voor de diagnostiek van patiënten met prostaatkanker, zowel bij primaire stadiëring als re-stadiëring. De techniek heeft een grotere accuratesse (92%; 95%-BI: 88-95) dan de voorheen gebruikte skeletscintigrafie (botscan) en CT (65%; 95%-BI: 60-69).2 Met name de specificiteit van de PSMA-PET-CT is erg hoog (98%; 95%-BI: 95-100); als er een afwijking zichtbaar is op de scan, betreft dit vrijwel altijd tumoractiviteit.2 Verder zijn er geen bijwerkingen gemeld van de PSMA-PET-CT.
Er bestaan verschillende PSMA-tracers. De meest gebruikte zijn gallium Ga-68-PSMA-tracers (bijvoorbeeld Ga-68-PSMA-HBED-CC, Ga-68-PSMA-11 en Ga-68-PSMA-I&T) en de fluor F-18-PSMA-tracers (bijvoorbeeld F-18-DCFPyL, F-18-DCFBC en F-18-PSMA-1007). Er zijn kleine verschillen tussen de PSMA-tracers, maar in diagnostische effectiviteit blijken ze niet veel van elkaar te verschillen.
Wat de klinische relevantie is van de grotere nauwkeurigheid van PSMA-PET-CT wordt nu onderzocht. De huidige behandelrichtlijnen zijn namelijk nog gebaseerd op studies waarin de oudere onderzoekstechnieken (botscan en CT) werden gebruikt. Dit ongemak werd al gesignaleerd bij de introductie van PSMA-PET zeven jaar geleden: wat te doen met de extra gevonden prostaatkankermetastasen? De patiënt wordt dan anders gestadieerd dan patiënten in grote therapie-trials die met conventionele beeldvorming uitgevoerd zijn en bij wie deze metastasen niet gevonden zouden zijn. Die discussie horen we regelmatig bij het multidisciplinaire overleg. Stadiëring met PSMA-PET-CT leidt er soms toe dat van een operatie wordt afgezien in verband met afstandsmetastasen die met conventionele beeldvormende technieken niet gedetecteerd waren.
Is de techniek kosteneffectief gebleken?
In een recente studie in Nederland is de kosteneffectiviteit van Ga-68-PSMA-PET-CT in de primaire diagnostiek van prostaatkanker vergeleken met die van conventionele diagnostiek.3 De gezondheidskosten en de effectiviteit – uitgedrukt in ‘quality-adjusted life years (qaly’s) – werden berekend over de levensduur. De uitkomst was dat de Ga-68-PSMA-PET-CT kostenbesparend was (€ 674 per patiënt), maar dat dat ten koste ging van een verlies qaly (0,011 qaly per patiënt). Het positieve effect kwam doordat patiënten geen ‘extended’ pelviene-lymfeklierdissectie (ePLND) hoefden te ondergaan als de Ga-68-PSMA-PET-CT afstandsmetastasen had laten zien. Het negatieve effect kwam doordat patiënten die eigenlijk potentieel curatief behandeld konden worden, voor een palliatief traject werden ingedeeld als met Ga-68-PSMA-PET-CT afstandsmetastasen waren gevonden. Een andere kosteneffectiviteitsstudie liet soortgelijke resultaten zien.4
Het is nog niet zeker of een ePLND voor de stadiëring van pelviene lymfekliermetastasen achterwege kan blijven als de Ga-68-PSMA-PET-CT geen metastasen laat zien, omdat de sensitiviteit daarvan laag is (85%; 95%-BI: 74-96).2 Dit wordt nu in een multicentrische studie onderzocht (PSMA-Select; NL9118).
Welke indicaties zijn er inmiddels?
Vanwege de grotere nauwkeurigheid is de PSMA-PET nu in nationale en internationale oncologische richtlijnen opgenomen als voorkeursmodaliteit bij de diagnostiek van prostaatkanker, naast de MRI voor de lokale beoordeling van de prostaat. In Nederland is de PSMA-PET-CT geïndiceerd bij de primaire diagnostiek van hoog-risicopatiënten voor de detectie van metastasen en als beeldvormend onderzoek geïndiceerd is bij een biochemisch recidief (PSA-waarden > 0,2 ng/ml) na prostatectomie of na radiotherapie (bron: richtlijn Prostaatcarcinoom). Hierbij vervangt PSMA-PET de skeletscintigrafie.
Verder wordt PSMA-PET-CT gebruikt om te beoordelen of patiënten met gemetastaseerde prostaatkanker in aanmerking komen voor behandeling met lutetium Lu-177-PSMA. Dit is een nieuwe therapie die gebaseerd is op hetzelfde principe van binding aan PSMA als de PSMA-PET-CT en waarmee prostaatkankercellen zeer lokaal bestraald kunnen worden. Een artikel over deze techniek verschijnt binnenkort in het NTvG.5
PSMA-PET-CT wordt in de meeste ziekenhuizen veelvuldig toegepast en per ziekenhuis worden jaarlijks enkele honderden van deze onderzoeken verricht. Van alle verrichtte PET-CT’s is ongeveer 5% een PSMA-PET-CT.
Literatuur
-
Lavalaye J, Lam MG, Verzijlbergen JF, Krijger GC, Vis R, de Keizer B. PSMA-PET voor prostaatkanker en eventuele metastasen. Ned Tijdschr Geneeskd. 2016;160:A9780 Medline.
-
Hofman MS, Lawrentschuk N, Francis RJ, et al; proPSMA Study Group Collaborators. Prostate-specific membrane antigen PET-CT in patients with high-risk prostate cancer before curative-intent surgery or radiotherapy (proPSMA): a prospective, randomised, multicentre study. Lancet. 2020;395:1208-16. doi:10.1016/S0140-6736(20)30314-7. Medline
-
Van der Sar ECA, Keusters WR, van Kalmthout LWM, et al. Cost-effectiveness of the implementation of [68Ga]Ga-PSMA-11 PET/CT at initial prostate cancer staging. Insights Imaging. 2022;13:132. doi:10.1186/s13244-022-01265-w. Medline
-
Scholte M, Barentsz JO, Sedelaar JPM, Gotthardt M, Grutters JPC, Rovers MM. Modelling study with an interactive model assessing the cost-effectiveness of (68)Ga prostate-specific membrane antigen positron emission tomography/computed tomography and nano magnetic resonance imaging for the detection of pelvic lymph node metastases in patients with primary prostate cancer. Eur Urol Focus. 2020;6:1967-74. Medline
-
Van Golen LW, Vogel W, Lam MGEH. Lutetium-177-PSMA bij gemetastaseerd prostaatcarcinoom. Ned Tijdschr Geneeskd. 2022;166:D6981 (ter perse).




Reacties