Toets voor nascholing (verlopen)
Aan dit artikel was een toets gekoppeld waarmee je nascholingspunten kon verdienen.
Samenvatting
- De incidentie van slokdarmkanker stijgt, vooral door een toename van het aantal adenocarcinomen in de distale slokdarm.
- Adeno- en plaveiselcelcarcinomen zijn de vaakst voorkomende histologische subtypes en moeten als verschillende entiteiten gezien worden.
- De diagnose ‘slokdarmkanker’ wordt gesteld op basis van histopathologisch onderzoek van biopten; tumorstadiëring wordt verricht met transoesofageale endo-echografie en FDG-PET/CT-onderzoek.
- Er zijn verschillende mogelijkheden om patiënten met slokdarmkanker te behandelen, zoals endoscopische resectie, multimodale therapie of definitieve chemoradiotherapie.
- Sinds 2012 is neoadjuvante chemoradiotherapie gevolgd door resectie de standaardbehandeling van slokdarmkanker, uitgezonderd bij patiënten met een T1- of M1-tumor.
- In Nederland worden tegenwoordig de meeste operaties minimaal invasief uitgevoerd.
- Ondanks betere behandelmogelijkheden, is de mortaliteit van slokdarmkanker nog altijd hoog.
artikel
Casussen
In het Amsterdam UMC krijgen 2 patiënten de uitslag van het PET-CT-onderzoek, nadat eerder bij hen slokdarmkanker is vastgesteld. Patiënt A is een 58-jarige, vitale man die aanvankelijk gewicht verloor en last kreeg van een gestoorde voedselpassage. Hij blijkt een cervicaal gelegen plaveiselcelcarcinoom te hebben. Patiënt B is een 71-jarige vrouw met onder andere overgewicht, atriumfibrilleren, COPD en reumatoïde artritis. Zij is doorverwezen vanuit een perifeer ziekenhuis voor de behandeling van een adenocarcinoom in de distale slokdarm. Het carcinoom was aan het licht gekomen na aanvullend onderzoek in het kader van langdurige refluxklachten en dyspepsie.
Uit de casussen bij dit artikel blijkt dat ‘de’ patiënt met slokdarmkanker niet bestaat en dat gepersonaliseerde zorg voor deze groep patiënten noodzakelijk is. In deze stand van zaken borduren wij voort op een eerder artikel over de diagnostiek en behandeling van niet-gemetastaseerde slokdarmkanker, dat in 2010 in dit tijdschrift verscheen. Wij zochten in PubMed en Embase naar revelante artikelen. Daarbij maakten wij gebruik van onder andere de volgende zoektermen: ‘oesophagus AND carcinoma’, ‘staging’, ‘treatment’, ‘(neo)adjuvant therapy’, ‘minimally invasive’, ‘RAMIE’, ‘cost effectivity’ en ‘quality of life/PROM’. Ook raadpleegden wij gegevens van de ‘Dutch Upper GI Cancer Audit’ (DUCA).
Epidemiologie
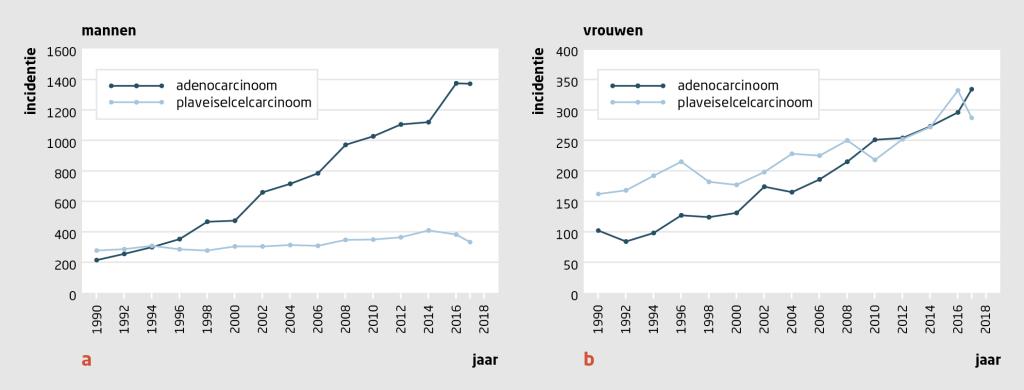
De incidentie van slokdarmkanker in Nederland is aanzienlijk gestegen, van 813 nieuwe gevallen in 1990 naar 2520 nieuwe gevallen in 2018 (figuur 1; www.ikcnet.nl). Mede door de multidisciplinaire en multimodale behandeling is de overleving van patiënten met slokdarmkanker in de afgelopen jaren verbeterd. Toch overlijden nog veel patiënten aan de gevolgen van slokdarmkanker. De prognose van patiënten met slokdarmkanker is sterk afhankelijk van het ziektestadium ten tijde van de diagnosestelling, tumorkenmerken, de respons op neoadjuvante behandeling en eventuele comorbiditeit. Mede doordat symptomen pas in een laat stadium optreden, is slechts de helft van de patiënten nog curatief te behandelen op het moment dat zij zich voor het eerst presenteren. De 5-jaarsoverleving van stadium 1-tumoren steeg van 33% in de periode 1989-1992 naar 60% in de periode 2011-2015. Voor stadium 2- en stadium 3-tumoren steeg de 5-jaarsoverleving respectievelijk van 17 en 7% naar 37 en 27%.1
Etiologie
Slokdarmkanker is onder te verdelen in verschillende histologische subtypes. Adeno- en plaveiselcelcarcinomen komen het vaakst voor. Hoewel er wat betreft de behandeling nog nauwelijks onderscheid wordt gemaakt tussen deze 2 subtypes, zijn er wel verschillen in risicofactoren, lokalisatie, moleculaire kenmerken en prognose. Recentelijk liet een uitgebreide moleculaire typering van 164 slokdarmtumoren zien dat er grote verschillen bestaan tussen beide subtypes en dat het adenocarcinoom van de slokdarm in sterke mate overeenkomt met het chromosomaal instabiele type adenocarcinoom van de maag.2 Plaveiselcelcarcinomen zijn juist meer verwant aan hoofd-halstumoren en kenmerken zich door amplificatie van CCND1, SOX2 of TP63.
De incidentiestijging van slokdarmkanker in de westerse wereld is vooral het gevolg van het toenemende aantal adenocarcinomen in de distale slokdarm. De belangrijkste risicofactor voor het ontwikkelen van een adenocarcinoom is een Barrett-oesofagus, een aandoening waarbij het plaveiselepitheel van de slokdarm wordt vervangen door metaplastisch cilinderepitheel. Jaarlijks ontwikkelt 0,3-0,5% van de patiënten met een Barrett-oesofagus hieruit een adenocarcinoom.3 Andere risicofactoren zijn: mannelijk geslacht, blank ras, gastro-oesofageale refluxziekte, roken en centrale obesitas. Hoewel de toename van obesitas en refluxziekte vermoedelijk bijdraagt aan de incidentiestijging van het adenocarcinoom, is er geen overtuigend bewijs dat een interventie die gericht is op deze risicofactoren het risico op het ontwikkelen van een adenocarcinoom daadwerkelijk verlaagt.4,5 Bij adenocarcinomen die gelokaliseerd zijn op de overgang tussen maag en slokdarm (zogenoemde ‘junction’-tumoren) kan sprake zijn van microsatellietinstabiliteit of een Epstein-Barr-virusinfectie. Plaveiselcelcarcinomen komen met name voor in het bovenste en middelste deel van de slokdarm en zijn in de westerse wereld sterk gerelateerd aan roken en alcoholmisbruik.
Diagnostiek
Bij patiënten met alarmsymptomen, zoals dysfagie, gewichtsverlies, braken, hematemesis of anemie, in combinatie met refluxklachten of dyspepsie wordt in de eerste plaats een oesofagogastroduodenoscopie met biopten verricht. Wanneer bij histopathologisch onderzoek van het biopt een slokdarmcarcinoom wordt gevonden, is aanvullend onderzoek vereist.
Transoesofageale endo-echografie kan aangewend worden om te bepalen of de tumor doorgroeit in de slokdarmwand en omliggende weefsels (sensitiviteit: 81,6-92,4%).6 Middels CT-onderzoek van de thorax en het abdomen kan beoordeeld worden of er afstandsmetastasen zijn. Tegenwoordig wordt het CT-onderzoek gecombineerd met FDG-PET-onderzoek. Bij 3-28% van de patiënten worden namelijk bij FDG-PET/CT-onderzoek afstandsmetastasen gevonden die op een gewone CT-scan niet zichtbaar zijn.7 Eventuele metastasering naar de lymfeklieren kan opgespoord worden met transoesofageale endo-echografie, CT-onderzoek of FDG-PET/CT-onderzoek (gecombineerde sensitiviteit: 83%). In sommige ziekenhuizen wordt als toevoeging hierop standaard cytologisch onderzoek van een dunnenaaldaspiraat en echografie van de hals uitgevoerd.8-10
Op basis van de bevindingen wordt een behandelplan opgesteld in een multidisciplinair overleg. Aan dit overleg nemen onder andere chirurgen, medisch oncologen, radiotherapeuten, mdl-artsen, pathologen, nucleair geneeskundigen, radiologen en verpleegkundig specialisten deel.
Behandeling
Er zijn verschillende behandelmogelijkheden, zoals endoscopische resectie, multimodale therapie (bestaande uit neoadjuvante chemoradiotherapie, gevolgd door een chirurgische resectie) of definitieve chemoradiotherapie.
Endoscopische resectie
Endoscopische resectie door de mdl-arts is een optie voor patiënten bij wie de slokdarmtumor slechts doorgroeit tot in de mucosa. Bij meer dan 95% van deze patiënten kan de tumor radicaal verwijderd worden middels endoscopische resectie en radiofrequente ablatie van het omliggende weefsel.3 Wanneer bij histopathologisch onderzoek van het resectiepreparaat blijkt dat de tumor toch verder doorgroeit dan de mucosa of wanneer er sprake is van lymfangio-invasie of een positief verticaal resectievlak, kan alsnog een slokdarmresectie worden uitgevoerd, eventueel voorafgegaan door neoadjuvante chemoradiotherapie.3,8
Multimodale therapie
Bij patiënten bij wie de slokdarmtumor verder doorgroeit dan de mucosa is een slokdarmresectie met een lymfeklierdissectie de aangewezen behandeling. Uit de CROSS-trial is gebleken dat neoadjuvante chemoradiotherapie (wekelijkse behandeling met paclitaxel en carboplatine in combinatie met bestraling met een dosis van 41,4 Gy in fracties van 1,8 Gy), gevolgd door een chirurgische resectie, tot een betere overleving leidt dan alleen een chirurgische resectie.11 Tegenwoordig krijgt 87% van de patiënten met slokdarmkanker in Nederland eerst chemoradiotherapie alvorens zij geopereerd worden.12
De overlevingswinst door neoadjuvante chemoradiotherapie geldt voor zowel het adeno- als het plaveiselcarcinoom.13 Niettemin blijft de vraag bestaan of patiënten met een adenocarcinoom wellicht meer baat hebben bij chemotherapie dan chemoradiotherapie. In de ESOPEC-trial wordt momenteel onderzocht of perioperatieve chemotherapie met 5-fluoro-uracil, folinezuur, oxaliplatine en docetaxel bij patiënten met een adenocarcinoom leidt tot een betere overleving dan chemoradiotherapie volgens het onderzoeksprotocol van de CROSS-trial.14,15
Na de neoadjuvante chemoradiotherapie kan een FDG-PET/CT-scan worden verricht om eventuele intervalmetastasen op te sporen. Middels FDG-PET/CT-onderzoek wordt bij circa 8% van de patiënten in de periode tussen de neoadjuvante chemoradiotherapie en de chirurgische behandeling een metastase ontdekt.16 Omdat genezing dan vaak niet meer mogelijk is, kan een belastende operatie achterwege gelaten worden. De kans op een fout-positieve bevinding bij FDG-PET/CT-onderzoek in het kader van ‘restaging’ is 5%, en daarom is het aan te bevelen om de aanwezigheid van een metastase te bevestigen middels histopathologisch onderzoek.
Recentelijk werd in een fase II-studie onderzocht wat het effect is van een behandelstrategie bestaande uit chemoradiotherapie, gevolgd door een afwachtend beleid.17 Een aanvullende slokdarmresectie vond alleen plaats in geval van een incomplete respons of een recidief. Van de 43 geïncludeerde patiënten was 37% nog in leven na 7 jaar. De onderzoekers concludeerden dat met deze behandelstrategie bij 49% van de patiënten een operatie voorkómen kon worden. Het effect van deze aanpak op de overleving wordt momenteel verder onderzocht in de SANO-trial.18 In deze trial worden patiënten geïncludeerd bij wie op basis van oesofagogastroduodenoscopie met biopten, transoesofageale endo-echografie met een dunnenaaldaspiratie en FDG-PET/CT-onderzoek een complete respons op neoadjuvante chemoradiotherapie verwacht wordt. Deelnemers worden gerandomiseerd tussen een afwachtend beleid of een chirurgische resectie.
Het doel van de huidige PRIDE-studie is om een predictiemodel te maken waarmee op basis van herhaald MRI-onderzoek, FDG-PET/CT-onderzoek, circulerend tumor-DNA en endoscopie met biopten voorspeld kan worden bij welke patiënten een complete respons op neoadjuvante chemoradiotherapie optreedt.19
Definitieve chemoradiotherapie
Definitieve chemoradiotherapie is een optie voor inoperabele patiënten of voor patiënten met een tumor die irresectabel is omdat deze gelegen is in het cervicale deel van de slokdarm – het korte deel tussen het cartilago cricoidea en de suprasternale inkeping – of omdat deze doorgroeit in omliggende structuren als de aorta of de bronchi.20,21 Uit de RTOG 85-01-trial is gebleken dat definitieve chemoradiotherapie (behandeling met cisplatine en 5-fluoro-uracil in combinatie met bestraling met een dosis van 50 Gy) een duidelijk overlevingsvoordeel biedt ten opzichte van alleen radiotherapie (bestraling met een dosis van 64 Gy).22 Sinds deze trial is 50,4 Gy de standaarddosis voor bestraling in het kader van definitieve chemoradiotherapie. Een Nederlandse retrospectieve cohortstudie onder 4501 75-plussers liet zien dat met name plaveiselcelcarcinomen goed reageren op chemoradiotherapie.23
Er is discussie over de optimale behandeling van patiënten met een plaveiselcelcarcinoom van de slokdarm. In een gerandomiseerde studie werd bij relatief fitte patiënten het effect van definitieve chemoradiotherapie vergeleken met dat van neoadjuvante chemoradiotherapie, gevolgd door een chirurgische resectie.24 De 2-jaarsoverleving was 35,4% in de groep patiënten die definitieve chemoradiotherapie onderging en 39,9% in de groep patiënten bij wie chemoradiotherapie en een chirurgische resectie werd uitgevoerd.
Om de overleving van patiënten met slokdarmkanker te verbeteren wordt momenteel veel onderzoek verricht naar de ontwikkeling van resistentie tegen chemoradiotherapie’.25 Een beter begrip van de tumorkenmerken leidt mogelijk tot de ontwikkeling van biomarkers, die gebruikt kunnen worden om patiënten te selecteren die dusdanig goed op de chemoradiotherapie zullen reageren dat ze niet meer geopereerd hoeven te worden. Ook kan dit onderzoek bijdragen aan de ontwikkeling van alternatieve adjuvante en neoadjuvante behandelstrategieën.
In een uitgebreide meta-analyse naar prognostische biomarkers voor patiënten met een resectabel adenocarcinoom van de slokdarm kwam naar voren dat met name immunologische kenmerken, zoals de expressie van ‘programmed death-ligand 1’ (PD-L1), gerelateerd zijn aan een slechte prognose.26 Immunotherapie, waaronder behandeling die gericht is op PD-L1, leidt mogelijk tot een betere overleving. Momenteel wordt in de PERFECT-studie onderzocht of het zinvol is om atezolizumab (anti-PD-L1) toe te voegen aan neoadjuvante chemoradiotherapie.
Dosisescalatie
Er zijn verschillende trials verricht naar de waarde van dosisescalatie. In de INT 0123-trial werd het effect van definitieve chemoradiotherapie (behandeling met cisplatine en 5-fluoro-uracil in combinatie met bestraling met een dosis van 64,8 Gy) vergeleken met dat van hetzelfde chemotherapieregime in combinatie met bestraling met een dosis van 50,4 Gy.27 De trial werd echter vroegtijdig beëindigd vanwege de hoge mortaliteit in de groep patiënten die bestraald werd met een dosis van 64,8 Gy. Er was geen overlevingswinst voor dosisescalatie, een bevinding die wordt onderschreven door de resultaten van een groot landelijk databaseonderzoek.28 Binnenkort worden de resultaten verwacht van de Nederlandse ArtDeco-studie, waarin het effect van dosisescalatie naast chemotherapie volgens het onderzoeksprotocol van de CROSS-trial wordt onderzocht.
Chirurgie
Chirurgische benaderingen
Om een slokdarmcarcinoom chirurgisch te verwijderen kan de tumor zowel transhiataal als transthoracaal benaderd worden. Bij de transhiatale benadering wordt de slokdarm vanuit het abdomen door de hiatus oesophagei gereseceerd. Hierbij blijft de chirurg transabdominaal werken en wordt de thorax niet geopend. Het merendeel van de patiënten (87%) wordt echter via een transthoracale benadering geopereerd, omdat hierbij de thoracale lymfeklieren en bloc verwijderd kunnen worden of omdat de tumor hoog in de thorax gelegen is.12 Bij abdominaal gelegen tumoren heeft echter de transhiatale benadering de voorkeur; deze operatietechniek wordt de Orringer-procedure genoemd.
Bij de transthoracale benadering worden 2 operatietechnieken het vaakst uitgevoerd: de Ivor Lewis- of de McKeown-procedure. Bij de Ivor Lewis-procedure wordt de anastomose intrathoracaal aangelegd, terwijl dat bij de McKeown-procedure cervicaal plaatsvindt. In 2017 werd in Nederland bij 55% van de patiënten die een resectie ondergingen een thoracale anastomose aangelegd, en bij 42% een cervicale anastomose.12 Beide procedures hebben voor- en nadelen. De keuze wordt onder andere bepaald door de anatomische lokalisatie van de tumor (figuur 2).

Bij subcarinaal gelegen tumoren kan zowel voor de Ivor Lewis- als de McKeown-procedure gekozen worden. De McKeown-procedure is mogelijk technisch makkelijker uit te voeren; ook zijn naadlekkages wellicht makkelijker te behandelen met behulp van drainage via de halswond, vergeleken met de Ivor Lewis-procedure. De laatstgenoemde procedure gaat mogelijk gepaard met een lager percentage patiënten bij wie een naadlekkage optreedt, maar ook met ernstige complicaties, zoals mediastinitis en pleura-empyeem. In 2016 is in Nederland de ICAN-trial gestart, waarin 200 patiënten gerandomiseerd worden tussen beide procedures.29 De primaire uitkomstmaten zijn het naadlekkagepercentage en postoperatieve morbiditeit, mortaliteit en kwaliteit van leven. De inclusieperiode eindigt naar verwachting in oktober 2019.
Minimaal invasieve chirurgie
Tegenwoordig wordt 91% van de slokdarmresecties in Nederland minimaal invasief uitgevoerd.12 In 2011 gold dit nog maar voor 31% van de operaties. Uit de TIME-trial is gebleken dat het voor de kwaliteit van de resectie en de 3-jaarsoverleving (40,4 vs. 50,5%; p > 0,05) niet uitmaakt of patiënten een open of minimaal invasieve slokdarmresectie ondergaan.30 Wel werden statistisch significant minder pulmonale complicaties gezien na minimaal invasieve chirurgie (34 vs. 12%).31 Een recente meta-analyse van 57 studies bevestigde de voordelen van minimaal invasieve chirurgie: minder bloedverlies, een kortere opnameduur, minder complicaties en een lagere mortaliteit. Het percentage patiënten met een naadlekkage was gelijk tussen patiënten die een open of minimaal invasieve slokdarmresectie ondergingen.32
Tot slot
De incidentie van slokdarmkanker in de westerse wereld neemt toe, en de mortaliteit van slokdarmkanker is nog altijd hoog, ondanks betere behandelmogelijkheden.
Omdat slokdarmkanker een grote impact heeft op de kwaliteit van leven, verdienen patiënten met deze ziekte een individuele benadering.33 Centralisatie van de zorg leidt tot op zekere hoogte tot meer expertise, betere behandeluitkomsten en dus tot meer geïndividualiseerde zorg.34 Ook een multidisciplinaire aanpak leidt tot betere behandelresultaten.35 Mede door de multidisciplinaire en multimodale behandeling is de overleving van patiënten met slokdarmkanker in de afgelopen jaren verbeterd. In het onderzoek naar slokdarmkanker wordt steeds meer aandacht besteed aan geïndividualiseerde zorg: welke patiënten zijn wel en welke patiënten zijn niet gebaat bij een bepaalde behandeling?
Naleving van de richtlijnen van Stichting Oncologische Samenwerking helpt om de kwaliteit van de zorg voor patiënten met slokdarmkanker te waarborgen. In de ‘Dutch Upper GI Cancer Audit’ worden de resultaten van de chirurgische behandeling van slokdarmkanker geregistreerd. Daarmee wordt inzicht verkregen in de kwaliteit van de slokdarmkankerzorg in Nederland en kunnen verbetertrajecten in gang gezet worden.
Literatuur
Integraal Kankercentrum Nederland.www.cijfersoverkanker.nl, geraadpleegd op 14 juni 2019.
Cancer Genome Atlas Research Network; Analysis Working Group: Asan University; BC Cancer Agency, et al. Integrated genomic characterization of oesophageal carcinoma. Nature. 2017;541:169-75.doi:10.1038/nature20805.Medline
Richtlijn Barrett-oesofagus. Haarlem: Nederlandse Vereniging van Maag-Darm-Leverartsen; 2018.
Coleman HG, Xie SH, Lagergren J. The epidemiology of esophageal adenocarcinoma. Gastroenterology. 2018;154:390-405.doi:10.1053/j.gastro.2017.07.046.Medline
Lagergren J, Smyth E, Cunningham D, Lagergren P. Oesophageal cancer. Lancet. 2017;390:2383-96.doi:10.1016/S0140-6736(17)31462-9.Medline
Puli SR, Reddy JB, Bechtold ML, Antillon D, Ibdah JA, Antillon MR. Staging accuracy of esophageal cancer by endoscopic ultrasound: a meta-analysis and systematic review. World J Gastroenterol. 2008;14:1479-90.doi:10.3748/wjg.14.1479. Medline
Van Westreenen HL, Westerterp M, Bossuyt PMM, et al. Systematic review of the staging performance of 18F-fluorodeoxyglucose positron emission tomography in esophageal cancer. J Clin Oncol. 2004;22:3805-12.doi:10.1200/JCO.2004.01.083.Medline
DaVee T, Ajani JA, Lee JH. Is endoscopic ultrasound examination necessary in the management of esophageal cancer? World J Gastroenterol. 2017;23:751-62.doi:10.3748/wjg.v23.i5.751. Medline
Van Vliet EPM, Heijenbrok-Kal MH, Hunink MGM, Kuipers EJ, Siersema PD. Staging investigations for oesophageal cancer: a meta-analysis. Br J Cancer. 2008;98:547-57.doi:10.1038/sj.bjc.6604200.Medline
Lerut T, Flamen P, Ectors N, et al. Histopathologic validation of lymph node staging with FDG-PET scan in cancer of the esophagus and gastroesophageal junction: a prospective study based on primary surgery with extensive lymphadenectomy. Ann Surg. 2000;232:743-52.doi:10.1097/00000658-200012000-00003. Medline
Van Hagen P, Hulshof MCCM, van Lanschot JJB, et al; CROSS Group. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med. 2012;366:2074-84.doi:10.1056/NEJMoa1112088. Medline
Jaarrapportage DUCA 2018.https://dica.nl/jaarrapportage-2018/duca, geraadpleegd op 21 juni 2019.
Sjoquist KM, Burmeister BH, Smithers BM, et al; Australasian Gastro-Intestinal Trials Group. Survival after neoadjuvant chemotherapy or chemoradiotherapy for resectable oesophageal carcinoma: an updated meta-analysis. Lancet Oncol. 2011;12:681-92.doi:10.1016/S1470-2045(11)70142-5.Medline
Al-Batran SE, Hofheinz RD, Pauligk C, et al. Histopathological regression after neoadjuvant docetaxel, oxaliplatin, fluorouracil, and leucovorin versus epirubicin, cisplatin, and fluorouracil or capecitabine in patients with resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4-AIO): results from the phase 2 part of a multicentre, open-label, randomised phase 2/3 trial. Lancet Oncol. 2016;17:1697-708.doi:10.1016/S1470-2045(16)30531-9.Medline
Hoeppner J, Lordick F, Brunner T, et al. ESOPEC: prospective randomized controlled multicenter phase III trial comparing perioperative chemotherapy (FLOT protocol) to neoadjuvant chemoradiation (CROSS protocol) in patients with adenocarcinoma of the esophagus (NCT02509286). BMC Cancer. 2016;16:503.doi:10.1186/s12885-016-2564-y. Medline
Kroese TE, Goense L, van Hillegersberg R, et al. Detection of distant interval metastases after neoadjuvant therapy for esophageal cancer with 18F-FDG PET(/CT): a systematic review and meta-analysis. Dis Esophagus. 2018;31:12.doi:10.1093/dote/doy055.Medline
Swisher SG, Moughan J, Komaki RU, et al. Final results of NRG Oncology RTOG 0246: an organ-preserving selective resection strategy in esophageal cancer patients treated with definitive chemoradiation. J Thorac Oncol. 2017;12:368-74.doi:10.1016/j.jtho.2016.10.002.Medline
Noordman BJ, Spaander MCW, Valkema R, et al; SANO study group. Detection of residual disease after neoadjuvant chemoradiotherapy for oesophageal cancer (preSANO): a prospective multicentre, diagnostic cohort study. Lancet Oncol. 2018;19:965-74.doi:10.1016/S1470-2045(18)30201-8.Medline
Borggreve AS, Mook S, Verheij M, et al; PRIDE study group. Preoperative image-guided identification of response to neoadjuvant chemoradiotherapy in esophageal cancer (PRIDE): a multicenter observational study. BMC Cancer. 2018;18:1006.doi:10.1186/s12885-018-4892-6.Medline
Mikhail S, Wei L, Salem ME, Bekaii-Saab T. Outcomes of definitive chemoradiation in patients with esophageal cancer. Dis Esophagus. 2017;30:1-7Medline.
Hoeben A, Polak J, Van De Voorde L, Hoebers F, Grabsch HI, de Vos-Geelen J. Cervical esophageal cancer: a gap in cancer knowledge. Ann Oncol. 2016;27:1664-74.doi:10.1093/annonc/mdw183.Medline
Herskovic A, Martz K, al-Sarraf M, et al. Combined chemotherapy and radiotherapy compared with radiotherapy alone in patients with cancer of the esophagus. N Engl J Med. 1992;326:1593-8.doi:10.1056/NEJM199206113262403. Medline
Koëter M, van Putten M, Verhoeven RHA, Lemmens VEPP, Nieuwenhuijzen GAP. Definitive chemoradiation or surgery in elderly patients with potentially curable esophageal cancer in the Netherlands: a nationwide population-based study on patterns of care and survival. Acta Oncol. 2018;57:1192-200.doi:10.1080/0284186X.2018.1450521. Medline
Stahl M, Stuschke M, Lehmann N, et al. Chemoradiation with and without surgery in patients with locally advanced squamous cell carcinoma of the esophagus. J Clin Oncol. 2005;23:2310-7.doi:10.1200/JCO.2005.00.034. Medline
Ebbing EA, van der Zalm AP, Steins A, et al. Stromal-derived interleukin 6 drives epithelial-to-mesenchymal transition and therapy resistance in esophageal adenocarcinoma. Proc Natl Acad Sci USA. 2019;116:2237-42.doi:10.1073/pnas.1820459116.Medline
Creemers A, Ebbing EA, Pelgrim TC, et al. A systematic review and meta-analysis of prognostic biomarkers in resectable esophageal adenocarcinomas. Sci Rep. 2018;8:13281.doi:10.1038/s41598-018-31548-6.Medline
Minsky BD, Pajak TF, Ginsberg RJ, et al. INT 0123 (Radiation Therapy Oncology Group 94-05) phase III trial of combined-modality therapy for esophageal cancer: high-dose versus standard-dose radiation therapy. J Clin Oncol. 2002;20:1167-74.doi:10.1200/JCO.2002.20.5.1167.Medline
Brower JV, Chen S, Bassetti MF, et al. Radiation dose escalation in esophageal cancer revisited: a contemporary analysis of the National Cancer Data Base, 2004 to 2012. Int J Radiat Oncol Biol Phys. 2016;96:985-93.doi:10.1016/j.ijrobp.2016.08.016. Medline
Van Workum F, Bouwense SA, Luyer MD, et al. Intrathoracic versus cervical anastomosis after minimally invasive esophagectomy for esophageal cancer: study protocol of the ICAN randomized controlled trial. Trials. 2016;17:505.doi:10.1186/s13063-016-1636-2. Medline
Straatman J, van der Wielen N, Cuesta MA, et al. Minimally invasive versus open esophageal resection: three-year follow-up of the previously reported randomized controlled trial: the TIME trial. Ann Surg. 2017;266:232-236.doi:10.1097/SLA.0000000000002171. Medline
Biere SS, van Berge Henegouwen MI, Maas KW, et al. Minimally invasive versus open oesophagectomy for patients with oesophageal cancer: a multicentre, open-label, randomised controlled trial. Lancet. 2012;379:1887-92.doi:10.1016/S0140-6736(12)60516-9.Medline
Yibulayin W, Abulizi S, Lv H, Sun W. Minimally invasive oesophagectomy versus open esophagectomy for resectable esophageal cancer: a meta-analysis. World J Surg Oncol. 2016;14:304.doi:10.1186/s12957-016-1062-7. Medline
Noordman BJ, Verdam MGE, Lagarde SM, et al. Effect of neoadjuvant chemoradiotherapy on health-related quality of life in esophageal or junctional cancer: results from the randomized CROSS trial. J Clin Oncol. 2018;36:268-75.doi:10.1200/JCO.2017.73.7718. Medline
Henneman D, Dikken JL, Putter H, et al. Centralization of esophagectomy: how far should we go? Ann Surg Oncol. 2014;21:4068-74.doi:10.1245/s10434-014-3873-5.Medline
Stephens MR, Lewis WG, Brewster AE, et al. Multidisciplinary team management is associated with improved outcomes after surgery for esophageal cancer. Dis Esophagus. 2006;19:164-71.doi:10.1111/j.1442-2050.2006.00559.x. Medline





Reacties