Samenvatting
De nieuwe ‘tumor-first’-werkwijze voor genetische diagnostiek bij ovariumcarcinoom is erop gericht om vrouwen met een erfelijke aanleg voor deze tumor effectief en doelmatig op te sporen. De tumor-first-werkwijze houdt in dat het tumor-DNA van patiënten met ovariumcarcinoom bij diagnose onderzocht wordt op de aanwezigheid van pathogene varianten van onder andere de BRCA1- en BRCA2-genen. Alleen vrouwen met een afwijkende uitslag van deze tumor-DNA-test komen in aanmerking voor een DNA-onderzoek van bloedcellen, om een erfelijke aanleg op te kunnen sporen. De tumor-DNA-test geeft ook informatie over de effectiviteit van een aanvullende behandeling met PARP-remmers. De tumor-first-werkwijze bespaart zo tijd en zorgkosten. Deze werkwijze wordt momenteel landelijk geïmplementeerd. De aandacht gaat daarbij uit naar het verspreiden van kennis onder de betrokken zorgprofessionals over het aanvragen, interpreteren en vastleggen van de tumor-DNA-test én het bieden van ondersteuning. De landelijke implementatie kan de opsporing van een erfelijke aanleg bij ovariumcarcinoom verder verbeteren.
artikel
In Nederland krijgen elk jaar ruim 120.000 mensen de diagnose kanker.1 Ongeveer 5% van de mensen met kanker heeft een erfelijke aanleg die het risico op het ontstaan van de ziekte verhoogt.2 De opsporing van zo’n erfelijke aanleg is belangrijk. Wanneer een erfelijke aanleg ontdekt wordt, krijgt zowel de patiënt als zijn of haar familie de mogelijkheid om maatregelen te nemen om kanker vroegtijdig op te sporen of te voorkomen.
Erfelijke aanleg bij ovariumcarcinoom
De kans dat erfelijkheid een oorzaak is bij het ontstaan van kanker verschilt per type kanker. Voor ovariumcarcinoom – dat wil zeggen: epitheliale maligniteiten van het ovarium – is de kans op een erfelijke aanleg aanzienlijk hoger dan gemiddeld. Bij ongeveer 12-15% van de vrouwen met ovariumcarcinoom speelt een erfelijke aanleg een rol. De oorzaak is veelal een pathogene variant van BRCA1 of BRCA2. Deze varianten gaan gepaard met een sterk verhoogd risico op ovariumcarcinoom – en ook op mammacarcinoom. Veel minder frequent kunnen ook pathogene varianten van RAD51C, RAD51D, BRIP1 en PALB2 zorgen voor een licht tot matig verhoogd risico op ovariumcarcinoom.3,4 Conform de landelijke richtlijn komen alle vrouwen met ovariumcarcinoom in aanmerking voor erfelijkheidsonderzoek.5
Erfelijkheidsonderzoek wordt na verwijzing aangevraagd door de klinisch geneticus. Dit proces kan emotioneel belastend zijn voor patiënten en er zijn hoge zorgkosten aan verbonden. Genetische diagnostiek bij patiënten met ovariumcarcinoom kan doelmatiger met de nieuwe ‘tumor-first’-werkwijze.
De tumor-first-werkwijze
De kern van de tumor-first-werkwijze is dat van iedere patiënt met de diagnose ‘ovariumcarcinoom’ eerst het tumor-DNA wordt onderzocht (‘tumor-first’) op de aanwezigheid van pathogene varianten van de risicogenen BRCA1, BRCA2, RAD51C, RAD51D, BRIP1 en PALB2. Voorheen was de tumor-DNA-test technisch te complex, maar door vooruitgang in de diagnostiek kon in Nederland enkele jaren geleden de tumor-first-werkwijze voor genetische diagnostiek bij ovariumcarcinoom ontwikkeld worden. Dat was internationaal baanbrekend.6,7
Het doel van de geavanceerde tumor-DNA-test is tweeledig. Ten eerste is de test een pre-test voor de selectie van patiënten die in aanmerking komen voor erfelijkheidsonderzoek. Bij de meeste patiënten – ruim 80% – wordt geen pathogene variant gevonden in het tumor-DNA. Voor hen is een verwijzing naar de klinisch geneticus niet nodig, tenzij de familieanamnese daar aanleiding toe geeft. De patiënten bij wie wél een pathogene variant wordt gevonden in het tumor-DNA – ongeveer 20% – komen in aanmerking voor een DNA-test op cellen in het bloed om pathogene varianten in de kiembaan te kunnen detecteren. Zij krijgen een verwijzing naar de klinisch geneticus aangeboden. Bij ruim de helft van de patiënten blijkt het om een erfelijke pathogene variant te gaan (pathogene kiembaanvariant; zie de Uitleg), terwijl de pathogene variant bij de anderen is opgetreden tijdens de kankerontwikkeling (pathogene somatische variant).6,7
Ten tweede geeft de tumor-DNA-test informatie over de effectiviteit van een aanvullende medicamenteuze behandeling met zogenoemde PARP-remmers. PARP-remmers voorkómen het herstel van beschadigde tumorcellen. Deze medicijnen zijn het effectiefst bij patiënten met een tumor die niet meer in staat is om dubbelstrengs DNA-breuken te repareren door een pathogene variant van BRCA1/2 (dit noemen we homologe-recombinatie-deficiënte tumoren).8,9
De tumor-first-werkwijze is multidisciplinair, zoals weergegeven in de figuur. De behandelaar – veelal de gynaecologisch oncoloog of een gynaecoloog met oncologie als aandachtsgebied – informeert de patiënte en gaat na of zij bezwaar heeft tegen een analyse van weefsel waarmee een verhoogde kans op een erfelijke aanleg voor ovariumcarcinoom kan worden aangetoond. Als de patholoog bij de beoordeling van het weefsel de diagnose ‘ovariumcarcinoom’ stelt en de patiënt geen bezwaar heeft, vraagt de patholoog een tumor-DNA-test aan. Die test wordt door een klinisch moleculair bioloog in de pathologie (KMBP) in nauwe afstemming met een laboratoriumspecialist klinische genetica (LSKG) beoordeeld, geïnterpreteerd en gerapporteerd. Vervolgens wordt de uitslag teruggekoppeld aan de hoofdbehandelaar en vastgelegd in het elektronisch patiëntendossier. De hoofdbehandelaar brengt de patiënt op de hoogte van de uitslag en de consequenties. De patiënt wordt verwezen naar een klinisch geneticus als er in het tumor-DNA een afwijking gevonden is of als de familieanamnese daar aanleiding toe geeft.
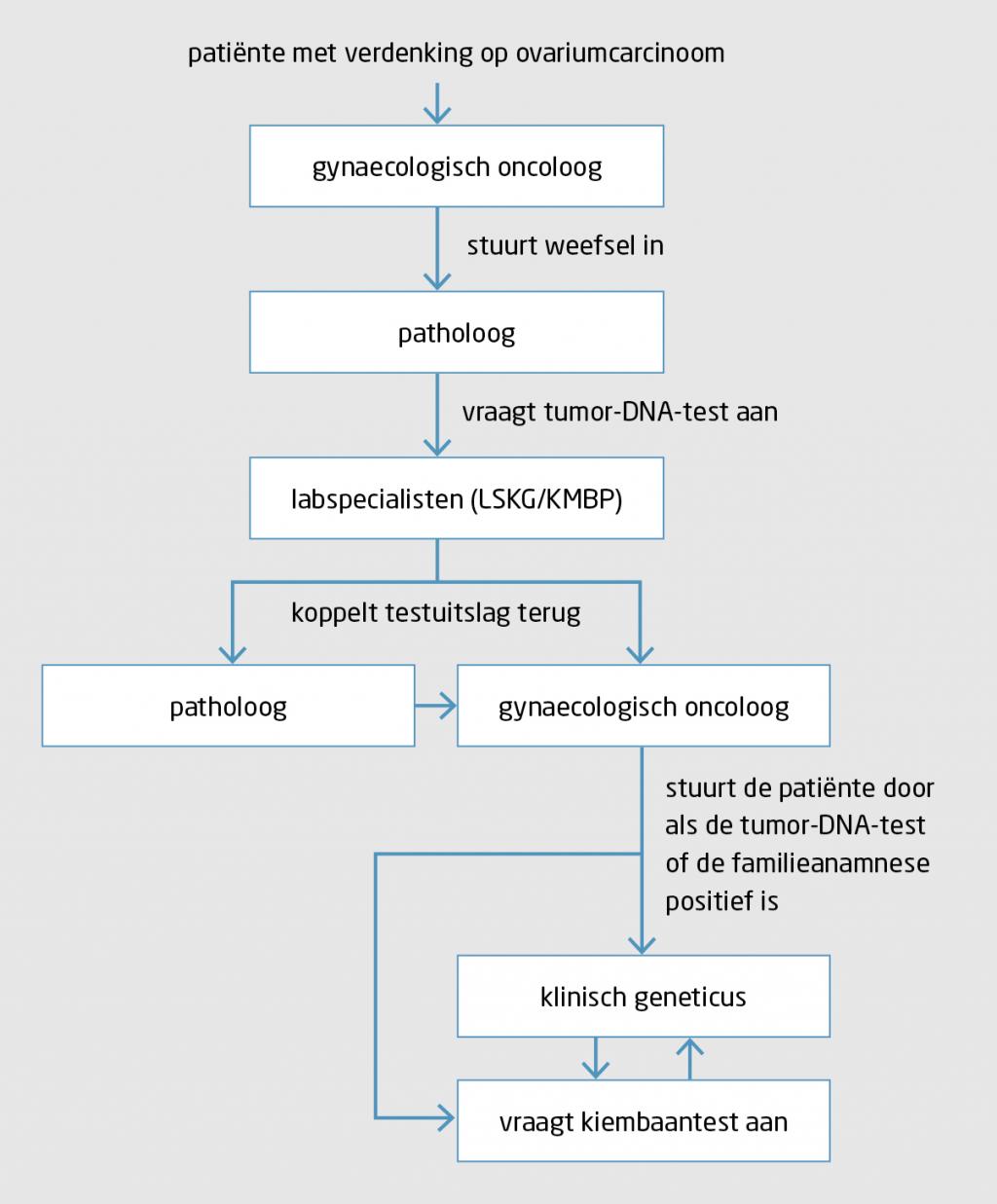
De voordelen van ‘tumor-first’
Door eerst het tumor-DNA te testen kan een erfelijke aanleg voor ovariumcarcinoom op een efficiënte en gerichte manier opgespoord worden. Bij ongeveer 80% van de patiënten met een ovariumcarcinoom is er immers geen indicatie voor een verwijzing naar de klinisch geneticus omdat de tumor-DNA-test niet afwijkend is. Deze aanpak bespaart dus tijd en zorgkosten en voorkomt een emotionele belasting van veel patiënten door het erfelijkheidsonderzoek.
Verder is het patiëntgericht om het tumor-DNA eerst te testen. Het oude advies om álle patiënten met een ovariumcarcinoom naar de klinisch geneticus te verwijzen, blijkt in de praktijk moeilijk uitvoerbaar; een meta-analyse laat zien dat het percentage patiënten dat daadwerkelijk getest wordt, laag is.10 Uit eerdere ervaringen blijkt echter dat systematische tumor-DNA-testen in de praktijk goed te implementeren zijn.6,7 Mogelijk kan dit zelfs sociaal-demografische verschillen in erfelijkheidsonderzoek verminderen.
Dankzij deze praktische haalbaarheid wordt er meer getest en kunnen met de tumor-first-werkwijze meer vrouwen met een erfelijke aanleg voor ovariumcarcinoom opgespoord worden. Hierdoor krijgen ook meer familieleden de mogelijkheid om zich te laten testen. Aan familieleden met een erfelijke aanleg kan een risico-reducerende salpingo-oöforectomie worden geadviseerd om ovariumcarcinoom te voorkómen.5,11 De vrouwen die een pathogene variant van BRCA1 of BRCA2 hebben, kunnen ook kiezen voor preventieve chirurgie of surveillance om mammacarcinoom te voorkómen of vroegtijdig op te sporen.11,12
Landelijke implementatie
Regionale implementatie van de tumor-first-werkwijze heeft laten zien dat deze werkwijze in de praktijk effectief en haalbaar is.6,7 Landelijke implementatie van de werkwijze bij ovariumcarcinoom is gewenst om regionale kwaliteitsverschillen in de zorg te voorkomen. Deze landelijke implementatie gaat echter niet vanzelf. Momenteel wordt de tumor-first-werkwijze landelijk multidisciplinair ingevoerd via een implementatieproject dat in 2020 van start is gegaan en financieel wordt ondersteund door het KWF.
Tijdens multidisciplinaire focusgroepdiscussies en telefonische interviews is kenbaar gemaakt dat alle beroepsgroepen achter de landelijke implementatie van de tumor-first-werkwijze staan.13 Ook patiëntenorganisaties steunen de implementatie. In de focusgroepdiscussies kwam naar voren welke factoren belangrijk zijn voor de implementatie.13 Multidisciplinaire samenwerking is essentieel, en recentelijk is deze samenwerking in een groot deel van Nederland verwezenlijkt. Communicatie, zowel intercollegiaal als naar de patiënt, staat centraal in de optimalisatie van de werkwijze.
Kwaliteit van de tumor-DNA-test en samenwerking zijn cruciaal
Aangezien de tumor-DNA-test bij ovariumcarcinoom dient als pre-test voor erfelijkheidsonderzoek, is het hoofdzaak dat de test geen pathogene variant mist; anders gezegd: de sensitiviteit moet zo hoog mogelijk zijn. De kwaliteit van de tumor DNA-test is cruciaal en hoort vergelijkbaar te zijn met die van de erfelijkheidstesten op bloedcellen. Om de kwaliteit te waarborgen en landelijk zo uniform mogelijk te houden, hebben experts vanuit het implementatieproject een leidraad opgesteld voor het testen van tumor-DNA.14 De tumor-DNA-test en interpretatie daarvan moeten voldoen aan kwaliteitseisen en landelijke afspraken voor erfelijkheidsdiagnostiek. Daarom worden deze testen uitgevoerd in centra waarin de specialisten van de afdelingen Pathologie en Klinische Genetica nauw met elkaar samenwerken.
Ook de samenwerking tussen specialisten van regionale en centrale ziekenhuizen is essentieel. De diagnose ‘ovariumcarcinoom’ kan gesteld worden in een regionaal ziekenhuis, terwijl de tumor-DNA-test wordt uitgevoerd in een umc of het Nederlands Kanker Instituut. Bij de chirurgische behandeling is altijd een gynaecologisch oncoloog uit een expertisecentrum betrokken,15 maar de chemotherapeutische behandeling door een medisch oncoloog kan wel decentraal plaatsvinden. Het belang van intercollegiale communicatie reikt dus verder dan het eigen ziekenhuis.
Alertheid op tumor-first
Er vormen zich in Nederland oncologische netwerken waarin regionale ziekenhuizen samenwerken met een centraal ziekenhuis. Waar sommige regio’s al enkele jaren de tumor-first-werkwijze toepassen bij patiënten met ovariumcarcinoom, is de implementatie in andere regio’s pas zeer recent gestart. Het uiteindelijke doel is dat de tumor-first-diagnostiek wordt toegepast bij álle patiënten met ovariumcarcinoom.
Hiervoor is het belangrijk dat zorgprofessionals in alle Nederlandse ziekenhuizen op de hoogte zijn van de werkwijze. Alle gynaecologen en pathologen moeten alert zijn op het aanvragen van de tumor-DNA-test, en specialisten uit veel disciplines, waaronder medisch oncologen, moeten weten hoe zij de uitslag van de tumor-DNA-test moeten interpreteren. Ook voor huisartsen is het belangrijk te weten dat de tumor-DNA-test geïncorporeerd wordt in de genetische diagnostiek voor patiënten met ovariumcarcinoom. Patiënten en familieleden kunnen immers met vragen komen over de uitslag van de tumor-DNA-test en over een mogelijk erfelijk verhoogd risico. Het is van belang dat zowel professionals als patiënten het verschil tussen een pathogene variant in de kiembaan (erfelijk) en een pathogene somatische variant (niet-erfelijk) begrijpen (zie de Uitleg).
Voor de landelijke implementatie is het essentieel om kennis te verspreiden en ondersteuning te bieden aan zorgprofessionals bij het aanvragen en interpreteren van de tumor DNA-test en het vastleggen van de testuitslag. Informatie over de tumor-first-werkwijze bij ovariumcarcinoom en het implementatieproject is te vinden op de website www.tumorfirst.nl. Er is een digitale toolbox ontwikkeld met specifieke hulpmiddelen en vooral praktische handvatten voor zorgprofessionals. Hoe meer professionals de tumor-first-werkwijze bij ovariumcarcinoom toepassen, hoe meer vrouwen met een erfelijke aanleg geïdentificeerd kunnen worden, en hoe meer gevallen van kanker bij familieleden voorkómen kunnen worden.
Tot besluit
De ontwikkelingen in de moleculaire diagnostiek zijn afgelopen jaren snel gegaan. Deze diagnostische ontwikkelingen gaan soms gepaard met een verandering in de optimale werkwijze. De tumor-first-werkwijze bij ovariumcarcinoom is daar een voorbeeld van. Een landelijke implementatie kan voorkómen dat er regionale verschillen in de kwaliteit en routing van de moleculaire diagnostiek gaan optreden. Het is te verwachten dat ook in de toekomst nieuwe ontwikkelingen onderdeel gaan uitmaken van de standaarddiagnostiek, zowel bij ovariumcarcinoom – denk aan het testen op homologe-recombinatie-deficiëntie – als bij andere ziektebeelden. De aanpak en lessen uit het implementatietraject van de tumor-first-werkwijze dragen bij aan eenduidige, kwalitatief hoogstaande diagnostiek in Nederland.
Literatuur
-
Bron: Nederlandse Kankerregistratie (NKR). https://iknl.nl/nkr-cijfers, geraadpleegd in juli 2022.
-
Bron: Erfelijke aanleg voor kanker. www.erfelijkheid.nl/ziektes/erfelijke-aanleg-voor-kanker, geraadpleegd in augustus 2022.
-
Arts-de Jong M, de Bock GH, van Asperen CJ, Mourits MJE, de Hullu JA, Kets CM. Germline BRCA1/2 mutation testing is indicated in every patient with epithelial ovarian cancer: A systematic review. Eur J Cancer. 2016;61:137-45. doi:10.1016/j.ejca.2016.03.009. Medline
-
Suszynska M, Ratajska M, Kozlowski P. BRIP1, RAD51C, and RAD51D mutations are associated with high susceptibility to ovarian cancer: mutation prevalence and precise risk estimates based on a pooled analysis of ~30,000 cases. J Ovarian Res. 2020;13:50. doi:10.1186/s13048-020-00654-3. Medline
-
Richtlijn Erfelijk en Familiair Ovariumcarcinoom. Utrecht: Federatie Medisch Specialisten; 2022.
-
Vos JR, Fakkert IE, de Hullu JA, et al; OPA Working Group. Universal tumor DNA BRCA1/2 testing of ovarian cancer: prescreening PARPi treatment and genetic predisposition. J Natl Cancer Inst. 2020;112:161-9. doi:10.1093/jnci/djz080. Medline
-
De Jonge MM, Ruano D, van Eijk R, et al. Validation and implementation of BRCA1/2 variant screening in ovarian tumor tissue. J Mol Diagn. 2018;20:600-11. doi:10.1016/j.jmoldx.2018.05.005. Medline
-
González-Martín A, Pothuri B, Vergote I, et al; PRIMA/ENGOT-OV26/GOG-3012 Investigators. Niraparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med. 2019;381:2391-402. doi:10.1056/NEJMoa1910962. Medline
-
Moore K, Colombo N, Scambia G, et al. Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med. 2018;379:2495-505. doi:10.1056/NEJMoa1810858. Medline
-
Lin J, Sharaf RN, Saganty R, et al. Achieving universal genetic assessment for women with ovarian cancer: Are we there yet? A systematic review and meta-analysis. Gynecol Oncol. 2021;162:506-16. doi:10.1016/j.ygyno.2021.05.011. Medline
-
Informatiebrieven Oncogenetica. Vereniging Klinische Genetica Nederland. www.vkgn.org/voorlichting/informatiebrieven/oncogenetica, geraadpleegd in juli 2022.
-
Richtlijn Borstkanker. Utrecht: Federatie Medisch specialisten; geraadpleegd in juli 2022.
-
Witjes VM, Braspenning JCC, Hoogerbrugge N, et al. Healthcare professionals’ perspectives on implementation of universal tumor DNA testing in ovarian cancer patients: multidisciplinary focus groups. Fam Cancer. 16 mei 2022. doi:10.1007/s10689-022-00294-0. Medline
-
Bosse T, van Noesel C, Hogervorst F, Koole W, Dubbink EJ, Ligtenberg M. Leidraad Tumor-First testaanpak bij recent gediagnosticeerde ovariumcarcinoom patiënten. www.tumorfirst.nl/toolbox/leidraad, geraadpleegd op 22 november 2022.
-
Timmermans M, Schuurman MS, Ho VKY, et al. Centralization of ovarian cancer in the Netherlands: Hospital of diagnosis no longer determines patients’ probability of undergoing surgery. Gynecol Oncol. 2018;148:56-61. doi:10.1016/j.ygyno.2017.11.009. Medline




Reacties