Beste collega’s,
Een retroperitoneale bloeding kan ontstaan door een trauma of iatrogene schade, maar soms ook zonder duidelijke aanleiding. Zo’n ‘spontane’ retroperitoneale bloeding kan moeilijk te herkennen zijn. Dat illustreren wij aan de hand van drie casussen.
Samenvatting
Een spontaan retroperitoneaal hematoom is een bloeding in de retroperitoneale ruimte zonder voorafgaand trauma. De diagnosestelling wordt vaak vertraagd door de aspecifieke klinische presentatie. In dit artikel beschrijven we drie patiënten met een spontaan retroperitoneaal hematoom.
Patiënt A had een spontane bloeding rond de rechter m. iliopsoas bij antistollingsgebruik (trombocytenaggregratieremmer) en werd conservatief behandeld. Patiënt B had een spontane arteriële bloeding rond de rechter nier als gevolg van een onderliggend feochromocytoom. Hij werd endovasculair behandeld en gedurende de follow-up werden de rechter nier en bijnier operatief verwijderd. Bij patiënt C trad een spontane ruptuur op van de linker v. iliaca bij een trombosebeen links; ze overleed kort na een spoedlaparotomie.
Dit artikel laat zien dat het klinisch beeld, de oorzaken en de behandelstrategieën van spontane retroperitoneale bloedingen zeer uiteenlopend zijn. Ook met adequaat beeldvormend onderzoek kan het lastig zijn de onderliggende oorzaak te identificeren. Een tijdige diagnose is echter van belang voor een behandelmethode op maat: conservatief, endovasculair of open-chirurgisch.
Kernpunten
- Een spontaan retroperitoneaal hematoom is een niet-traumatische bloeding.
- De klinische presentatie, onderliggende oorzaken en behandelmethoden lopen uiteen.
- Overweeg de diagnose bij vage buikklachten en onverklaarde anemie.
- Ook met adequaat beeldvormend onderzoek kan het lastig zijn de onderliggende oorzaak van een spontaan retroperitoneaal hematoom vast te stellen.
- Tijdige herkenning van de onderliggende oorzaak is van belang voor een behandeling op maat: conservatief, endovasculair of open-chirurgisch.
artikel
Patiënt A is een 71-jarige man met in de voorgeschiedenis een ‘coronary artery bypass graft’ (CABG) en een ‘transient ischemic attack’ (TIA). Vanwege zijn voorgeschiedenis gebruikte hij carbasalaatcalcium (ascal). Verder werd hij behandeld vanwege erysipelas van het rechter been. Tijdens deze behandeling kreeg hij plotseling pijn in de rechter lies en doofheid en spierzwakte van het rechter been. Het rechter been was verdikt, maar wel soepel en niet extreem pijnlijk. Een CT-scan met intraveneus contrast liet een retroperitoneaal hematoom zien rond de rechter m. iliopsoas, zonder actieve bloeding. Omdat de patiënt hemodynamisch stabiel was, werd gekozen voor een expectatief beleid. De hemoglobineconcentratie was gedaald van 8,0 naar 5,5 mmol/l (referentiewaarden: 8,5-10,5).
Een dag later werd vanwege hypotensie en verminderde diurese opnieuw een CT-scan verricht. Ditmaal was wel een actieve retroperitoneale bloeding zichtbaar, maar zonder een duidelijk focus (figuur 1).
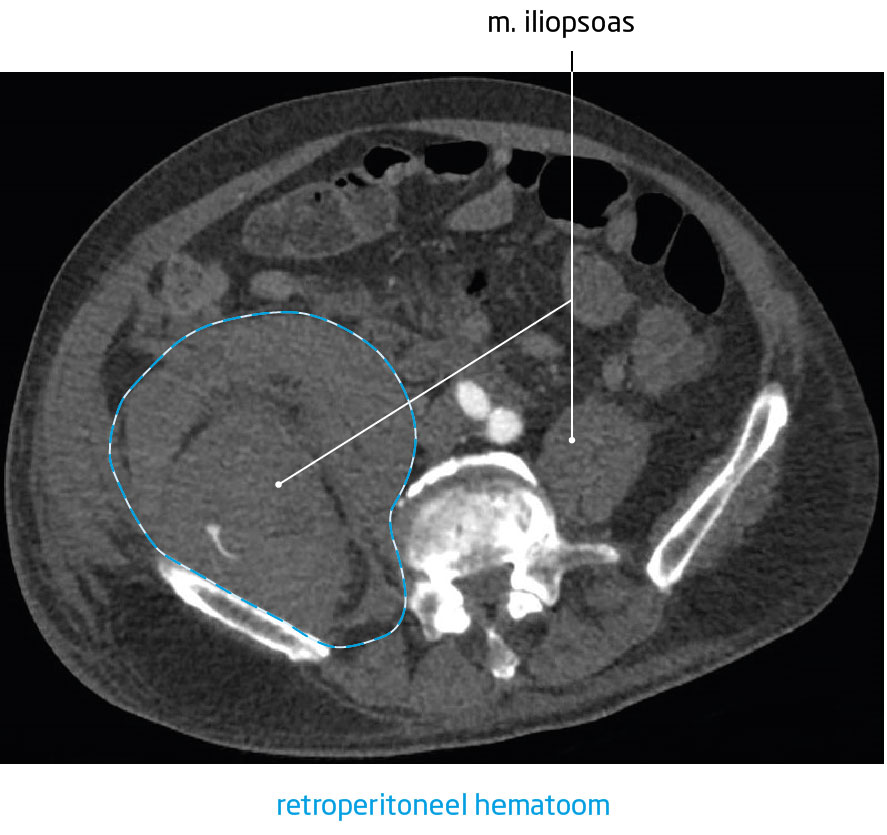
Patiënt A werd naar ons ziekenhuis gebracht voor verdere behandeling. Bij binnenkomst dienden wij drie erytrocytenconcentraten toe (‘packed cells’; PC’s). De patiënt was daarbij aanspreekbaar en hemodynamisch stabiel (bloeddruk 119/79 mmHg, pols 95/min). Bij lichamelijk onderzoek was er sprake van een abdominale zwelling en drukpijn in het rechter onderkwadrant.
We verrichtten angiografie onderzoek om het bloedingsfocus te lokaliseren en indien mogelijk direct te emboliseren. Daarbij zagen we echter geen actieve bloeding; embolisatie was dus niet nodig. Wij veronderstelden dat de bloeding inmiddels was getamponneerd en stelden daarom opnieuw een expectatief beleid in.
Nog diezelfde avond collabeerde de patiënt bij het opstaan, waarna hij direct goed aanspreekbaar was. Bij een Hb-concentratie van 4,5 mmol/l werden twee PC’s en tranexaminezuur toegediend; de dag erna volgde nog één extra PC. Nadien bleef de patiënt klinisch stabiel en herstelde hij van zijn erysipelas. Op de vierde opnamedag ging hij in klinische goede toestand en met een stabiel Hb (5,3 mmol/l) retour naar het verwijzend ziekenhuis.
Patiënt B, een 48-jarige man zonder relevante voorgeschiedenis, kwam op de SEH van een ander ziekenhuis met continue, stekende pijn in de rechter flank met misselijkheid en braken. De pijn was enkele uren eerder plotseling ontstaan. De patiënt had geen koorts en de mictie en ontlasting waren niet afwijkend. Zijn abdomen was gespannen met drukpijn in het rechter hemi-abdomen en de rechter flank. Een CT-scan met intraveneus contrast toonde een arteriële bloeding van de rechter bijnier (figuur 2). Hierna werd de patiënt met spoed naar ons ziekenhuis overgeplaatst. De patiënt was klam en bleek met een bloeddruk van 144/103 mmHg en een hartfrequentie van 124/min. De Hb-concentratie was 6,3 mmol/l.
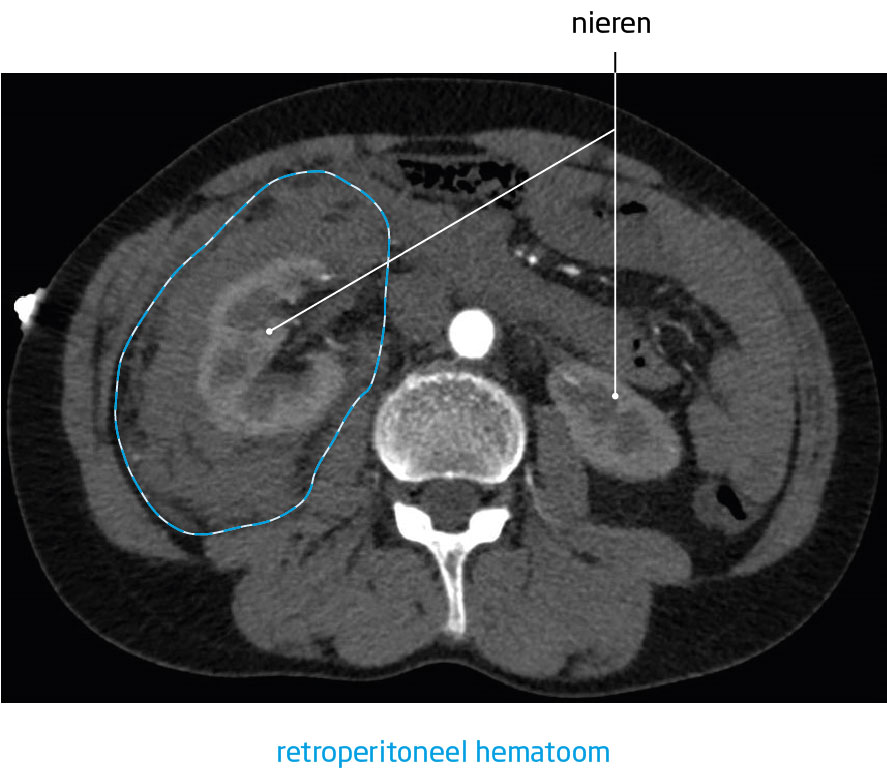
Wij verrichtten aanvullend angiografisch onderzoek onder anesthesiologische begeleiding om het bloedingsfocus in kaart te brengen. Er bleek sprake van een actieve bloeding in de rechter bijnierloge, wat kon passen bij een niertumor. Embolisatie van de rechter a. adrenalis en het distale deel van de a. phrenica verliep succesvol. Daarna was de patiënt hemodynamisch stabiel, al was de Hb-concentratie gedaald naar 4,7 en waren de cardiale markers in het bloed gestegen. De patiënt kreeg twee PC’s, waarna de Hb-concentratie stabiel bleef ( > 6,0 mmol/l). De verhoogde cardiale markers werden geduid als passend bij de doorgemaakte hypovolemische shock en de bijbehorende mismatch tussen de zuurstofvraag en het aanbod (type II-ischemie).
Tien dagen na ontslag werd de patiënt opgenomen vanwege een nieuwe episode van pijn in de rechter flank. Een CT-scan liet geen bloeding zien. De pijnmedicatie werd geoptimaliseerd en de patiënt werd in goede conditie naar huis ontslagen.
Als bloedingsoorzaak werd gedacht aan een bijniertumor in de vorm van een adenoom, feochromocytoom of carcinoom. De verhoogde plasmaconcentraties van normetanefrine pasten zowel bij een feochromocytoom als bij een fout-verhoogde uitslag, zoals bij stress. Poliklinische PET-scan bevestigde de diagnose feochromocytoom. De patiënt onderging een in opzet laparoscopische ‘en-bloc’-resectie van de rechter bijnier; vanwege veel fibrose en peri-tumorale inflammatie werd tijdens de operatie overgestapt op een open-chirurgische benadering.
Patiënt C, een 71-jarige vrouw zonder relevante voorgeschiedenis, kreeg plots een licht gevoel in het hoofd en pijn in de onderrug. Kort daarna verloor zij het bewustzijn, waarna omstanders haar reanimeerden.
Bij aankomst op de SEH was de patiënte geïntubeerd. Ze bleef hypotensief ondanks toediening van vocht, bloedproducten, atropine en adrenaline. Ze had een hartfrequentie van 40/min, een temperatuur van 33,4 °C en een Hb-concentratie van 3,3 mmol/l. Ze had een koude gemarmerde huid, soepel abdomen, palpabele liespulsaties en een gezwollen linker been.
Een CT-scan met contrast liet een uitgebreid retroperitoneaal hematoom zien rond de linker nier, zonder extravasatie van contrast. Derhalve bleek het cardiale arrest veroorzaakt door een hemorragische shock bij het vermoeden van een bloedende niertumor. Conservatieve behandeling zou gepaard gaan met snelle hemodynamische achteruitgang en een infauste prognose. Omdat endovasculaire behandeling niet mogelijk was, werd besloten om een spoedlaparotomie te verrichten.
De vaatchirurg en de uroloog voerde de operatie samen uit. Het gezwollen linker been duidden ze aanvankelijk als compressie van het hematoom op de linker v. iliaca externa. Perioperatief werd de retroperitoneale ruimte geopend en de aorta afgeklemd. Bij exploratie bleek de linker v. ovarica te zijn uitgescheurd ter hoogte van de linker v. renalis, vermoedelijk bij tractie door de massawerking van het hematoom. De vene werd geligeerd en de v. renalis overhecht waarna een linkszijdige nefrectomie plaatsvond om het vermoedelijke bloedingsfocus te stoppen. Macroscopisch was er sprake van een klein ruimte-innemend proces van de linker nier, zonder bloeding. Tegelijkertijd informeerde de interventieradioloog de operateurs dat bij herbeoordeling van de CT-scan de linker v. iliaca geruptureerd leek. Nadere chirurgische exploratie bracht inderdaad een forse scheur van de linker v. iliaca externa aan het licht. De ruptuur werd overhecht en de abdominale holte getamponneerd met gazen. Vervolgens bleef de bloeddruk dalen bij iedere poging om de aortaklem te verwijderen. Ondanks herhaaldelijke pogingen de patiënt te stabiliseren, overleed zij nog voor ze op de afdeling Intensive Care was gearriveerd.
Bij obductie was te zien dat de patiënte een linkszijdige nefrectomie had ondergaan, er sprake was van een uitgebreid retro- en intraperitoneaal hematoom en er hechtingen zaten in de linker v. renalis en v. ovarica. De weke delen rondom de v. iliaca lieten een hematoom zien dat tot in het linker been reikte. Er werd een ruptuur in de v. iliaca gezien ter plaatse van de hechtingen. Ook was er sprake van een trombus in de linker v. iliaca interna en de v. iliaca externa. Microscopisch werden organiserende trombi waargenomen in de v. iliaca communis, v. iliaca interna en v. iliaca externa sinistra, met aan de rand overwegend granulatieweefsel met re-vascularisatie.
Vanwege de langer bestaande trombi bij obductie dachten wij aan een diepe veneuze trombose (DVT) als oorzaak van de v.-iliacaruptuur. Een spontane ruptuur van de v. iliaca komt met name voor bij patiënten met een DVT.9 Bij onze patiënt waren er zowel klinische als radiologische aanwijzingen voor een DVT.
Beschouwing
In dit artikel beschreven wij drie patiënten met een spontaan retroperitoneaal hematoom. Deze casussen illustreren dat de behandeling afhangt van de oorzaak en of er sprake is van een actieve bloeding.1 Ook beschrijven ze de aspecifieke klinische presentatie van spontane retroperitoneale hematomen, waardoor de diagnose vaak wordt vertraagd.2
Hieronder gaan wij verder in op het wisselende klinisch beeld van retroperitoneale hematomen, de uiteenlopende oorzaken en verschillende behandelmethoden.
Spontane retroperitoneale bloedingen
Er zijn uiteenlopende oorzaken van spontane retroperitoneale hematomen, waarvan grofweg twee derde gerelateerd is aan antistolling.3 Andere oorzaken zijn zeldzamer, zoals tumoren, gynaecologische afwijkingen en spontane veneuze bloedingen. De klinische presentatie is ook gevarieerd: ongeveer twee derde van de patiënten heeft buikpijn, zo’n 20% pijn in de rug of benen, en minder dan 10% heeft een palpabele abdominale massa of een huidverkleuring van de buik, rug of flank. De presentatie kan acuut zijn met tekenen van een hemorragische shock, of subacuut met een onbegrepen anemie en buikpijn.1,3
De diagnose kan worden gesteld op basis van een CT-scan van het abdomen met intraveneus contrast, waarbij gescand dient te worden in de blanco, arteriële en veneuze fase. De behandeling is meestal conservatief.4
De exacte incidentie van spontane retroperitoneale hematomen is onbekend. De aandoening is zeldzaam; studies ernaar betreffen grotendeels patiëntbeschrijvingen, patiëntenseries of kleinere retrospectieve cohortstudies met hoogstens tientallen patiënten.2-5
Antistolling
Ruim twee derde van de spontane retroperitoneale hematomen treedt op bij patiënten die antistolling gebruiken.2,3 Bloedingen kunnen optreden bij gebruik van therapeutische anticoagulantia, zoals vitamine-K-antagonisten, laagmoleculairgewicht heparine en directe orale anticoagulantia, maar ook bij gebruik van een trombocytenaggregatieremmer.3-5
De conservatieve behandeling van patiënten met een spontaan retroperitoneaal hematoom bestaat uit een ziekenhuisopname ter observatie, het herstellen van de vullingsstatus (bloedproducten) en het couperen van de antistolling.2,5
In een eerdere studie overleden 11 patiënten met een spontaan retroperitoneaal hematoom, waarvan bij 5 patiënten sprake was van een ‘goed gecontroleerde bloeding’.2 Deze patiënten overleden niet direct als gevolg van het hematoom, maar door een aspiratiepneumonie, cardiovasculaire aandoening of cerebrovasculair accident.2 Het is aannemelijk dat deze sterftegevallen gerelateerd zijn aan kwetsbaarheid van de betreffende patiënten.
Arteriële bloedingen
Vanuit meerdere retroperitoneale structuren kan een bloeding ontstaan. Een bekende acuut verlopende oorzaak is een geruptureerd aneurysma van de aorta abdominalis, hoewel deze in de literatuur niet altijd als ‘spontaan’ wordt aangemerkt.2,3 Zeldzamer zijn bloedingen uit retroperitoneale arteriën.6
Met een CT-scan van het abdomen met intraveneus contrast kan de locatie en uitgebreidheid van de bloeding in kaart worden gebracht. Ook kan op basis hiervan worden bepaald of het een actieve bloeding betreft (extravasatie van contrast). De locatie van de bloeding helpt bij het vaststellen van de oorzaak, de uitgebreidheid ervan bij bepaling van de hoeveelheid bloedverlies en de eventuele extravasatie van contrast bij het overwegen van een ingreep.
Een endovasculaire behandeling is minimaal invasief en geniet de voorkeur. Open-chirurgische interventies kunnen overwogen worden bij afwezigheid van endovasculaire behandelmogelijkheden, bij persisterende hemodynamische instabiliteit of bij het vermoeden van een abdominaal compartimentsyndroom.4,7
Spontane v.-iliacarupturen
Er zijn verschillende hypotheses voor het ontstaan van spontane v.-iliacarupturen: mechanisch, inflammatoir en hormonaal.8 De mechanische hypothese is gerelateerd aan het syndroom van May-Thurner. Bij dit syndroom is er sprake van een verhoogde veneuze druk in het linker been en bekken, doordat de linker v. iliaca communis beklemd is tussen de ventraal kruisende rechter a. iliaca communis en dorsaal de vijfde lumbale wervel. De inflammatoire hypothese stelt dat de kans op ruptuur toeneemt doordat de vaatwand minder elastisch wordt als gevolg van chronische inflammatie na een DVT. De hormonale hypothese veronderstelt dat oestrogeen beschermt tegen vaatwandrupturen.
In de literatuur zijn 76 patiënten met een spontane v.-iliacaruptuur beschreven in 64 studies.9 Ruim 96% van de patiënten had een linkszijdige ruptuur, 84% was vrouw en 84% had gelijktijdig een DVT. De gemiddelde leeftijd was 61 jaar. Een spontane v.-iliacaruptuur moet daarom overwogen worden bij een linkszijdige retroperitoneale bloeding en een gelijktijdige DVT, in het bijzonder bij vrouwen van middelbare leeftijd of ouder. Bij 62% van de patiënten was de diagnose nog niet bekend na aanvullend beeldvormend onderzoek, maar werd die pas gesteld tijdens de behandeling.9
Zeker bij een veneuze oorzaak moet men terughoudend zijn in de open-chirurgische benadering van retroperitoneale hematomen, vooral als het focus onbekend is, tenzij het gaat om een uiterste poging in een situatie tussen leven en dood. De tabel geeft per oorzaak een globaal overzicht van de verschillende behandelstrategieën die overwogen kunnen worden. Iedere casus is echter uniek en verdient een behandeling op maat.

Beste collega’s, in dit artikel illustreerden wij de uiteenlopende klinische presentatie van spontane retroperitoneale hematomen, de diverse oorzaken en de verschillende behandelmethoden die overwogen moeten worden. Ook met de juiste beeldvormende onderzoeken kan het lastig zijn de onderliggende oorzaak vast te stellen. Een tijdige diagnose is echter van belang om een behandeling op maat te kunnen bieden. Die behandelmethode kan conservatief zijn, endovasculair of open-chirurgisch.
Literatuur
- Kasotakis G. Retroperitoneal and rectus sheath hematomas. Surg Clin North Am. 2014;94(1):71-76. doi:10.1016/j.suc.2013.10.007. Medline
- Baekgaard JS, Eskesen TG, Lee JM, et al. Spontaneous retroperitoneal and rectus sheath hemorrhage-management, risk factors and outcomes. World J Surg. 2019;43(8):1890-1897. doi:10.1007/s00268-019-04988-y. Medline
- Sunga KL, Bellolio MF, Gilmore RM, Cabrera D. Spontaneous retroperitoneal hematoma: etiology, characteristics, management, and outcome. J Emerg Med. 2012;43(2):e157-e161. doi:10.1016/j.jemermed.2011.06.006. Medline
- Lukies M, Gipson J, Tan SY, Clements W. Spontaneous retroperitoneal haemorrhage: efficacy of conservative management and embolisation. Cardiovasc Intervent Radiol. 2023;46(4):488-495. doi:10.1007/s00270-023-03359-4. Medline
- Sahu KK, Mishra AK, Lal A, George SV, Siddiqui AD. Clinical spectrum, risk factors, management and outcome of patients with retroperitoneal hematoma: a retrospective analysis of 3-year experience. Expert Rev Hematol. 2020;13(5):545-555. doi:10.1080/17474086.2020.1733963. Medline
- Tan EWK, Shelat VG, Monteiro AY, Low JK. Spontaneous retroperitoneal haemorrhage from pancreatoduodenal artery (PDA) rupture and associated complications. BMJ Case Rep. 2022;15(10):2022-250383. doi:10.1136/bcr-2022-250383. Medline
- Chan YC, Morales JP, Reidy JF, Taylor PR. Management of spontaneous and iatrogenic retroperitoneal haemorrhage: conservative management, endovascular intervention or open surgery? Int J Clin Pract. 2008;62(10):1604-1613. doi:10.1111/j.1742-1241.2007.01494.x. Medline
- Tannous H, Nasrallah F, Marjani M. Spontaneous Iliac vein rupture: case report and comprehensive review of the literature. Ann Vasc Surg. 2006;20(2):258-262. doi:10.1007/s10016-006-9003-5. Medline
- Kooiman AL, Bakas JM, van Fessem JMK, Boellaard WPA, Cornelissen SAP, van Rijn MJE. Spontaneous iliac vein ruptures: a systematic review. Vasc Endovascular Surg. 2023;57(6):617-625. doi:10.1177/15385744231163707. Medline




Reacties