Beste collega’s,
In deze klinische les gaan we het hebben over groep A-streptokokken. Deze bacterie kan veel verschillende ziektebeelden veroorzaken, variërend van faryngitis tot ernstige invasieve infecties, zoals puerperale sepsis, necrotiserende wekedeleninfecties en streptokokken-toxische-shocksyndroom. In 2022 was de incidentie van deze invasieve infecties hoger dan in voorgaande jaren. Wij beschrijven vier patiënten met zo’n invasieve groep A-streptokokkeninfectie.
Patiënt A, een voorheen gezonde 42-jarige vrouw, kwam naar de Spoedeisende Hulp (SEH), omdat ze sinds drie dagen een rood en gezwollen linker been had. Daarnaast had ze last van algehele malaise, hoofdpijn en buikpijn. De klachten waren verergerd ondanks behandeling met flucloxacilline oraal. Bij lichamelijk onderzoek was het hele been gezwollen en extreem pijnlijk bij aanraking. Er werd geen gebied met gevoelloosheid opgemerkt.
Op de SEH had de patiënte een tachycardie met een niet-afwijkende bloeddruk en een lichaamstemperatuur van 38,3 °C. Ze maakte een zieke indruk. De huid van de linker enkel was donkerpaars verkleurd en de gehele mediale zijde van het been had een scherpbegrensde roodheid; er was geen sprake van subcutane crepitaties (figuur 1). De laboratoriumuitslagen lieten met name sterk verhoogde infectieparameters zien (referentiewaarden tussen haakjes): CRP: 455 mg/l (< 10); leukocyten: 20,9 x 109/l (4-10).

Vanwege de verdenking op een necrotiserende wekedeleninfectie (NWDI) besloten wij…
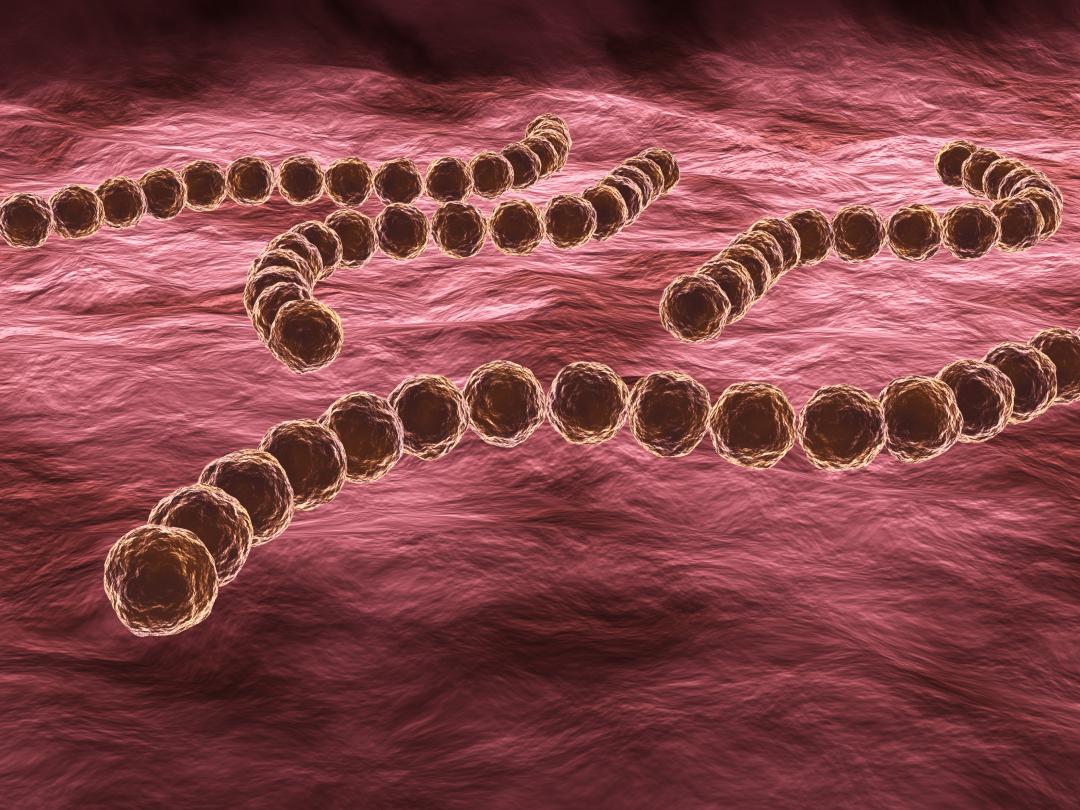



Uitbreiding meldplicht en profylaxe bij invasieve groep A-streptokokken
Graag vestigen we uw aandacht op de meest recente veranderingen in de richtlijnen ten aanzien van meldplicht en profylaxe voor huishoudcontacten van patiënten met invasieve groep A-streptokokken (iGAS).
Zoals het bovenstaande artikel beschrijft is het aantal gevallen met iGAS sinds de lente van 2022 hoger dan de jaren daarvoor.(1) Echter, sinds december 2022 wordt er landelijk een extra scherpe toename van invasieve infecties met groep A Streptokokken gerapporteerd.(2,3) Op dit moment is nog niet duidelijk waarom de iGAS infecties zo sterk toenemen. Mogelijke factoren zijn een verminderde expositie tijdens COVID-19 pandemie of een toename van S. pyogenes infecties met stammen met een verhoogd invasief potentieel, zoals eerder beschreven in een uitbraak in het Verenigd Koninkrijk van het M1UK type. Deze M1UK S. pyogenes stam kenmerkt zich door een toegenomen productie van exotoxines, waardoor er een uitgebreidere inflammatoire respons kan ontstaan.(4)
De Nederlandse richtlijn Groep A Streptokokkeninfecties beschouwde tot voor kort puerperale koorts/sepsis, het streptococcal toxic shock syndrom (STSS) en fasciitis necroticans als vormen van iGAS. Inmiddels is de definitie verbreed naar een meer internationaal geaccepteerde definitie: een kweek met GAS van een normaal steriele plek (bijvoorbeeld bloed, liquor, pleuravocht). (3,5)
Sinds 20 januari j.l. is de meldplicht verruimd naar alle vormen van iGAS, deze moeten binnen 1 dag (ook in het weekend) door de medisch microbioloog/behandeld arts gemeld worden bij de GGD. De nieuwe meldplicht omvat:
Tevens is het advies voor antibiotische profylaxe verruimd naar huishoudcontacten van patiënten met alle vormen van iGAS en niet meer beperkt tot de huishoudcontacten van patiënten met STSS en fasciitis necroticans op basis van een GAS infectie.(2,3) Chemoprofylaxe bestaat voor volwassenen uit azitromycine (3 dagen), clindamycine (10 dagen) of penicilline / feniticilline (10 dagen) in combinatie met 4 dagen rifampicine. Een huishoudcontact wordt hierbij gedefinieerd als een persoon die meer dan 24 uur het huishouden deelde met de index patiënt vanaf 7 dagen voor ontstaan van de ziekte bij de index patiënt, tot 24 uur na start van antibiotische behandeling.(3)
Gezins- en huishoudcontacten blijken een verhoogd risico te hebben op iGAS, waarbij de GAS infectie kan “pingpongen” tussen de verschillende familieleden.(6) In een Engelse retrospectieve cohort studie bleek het absolute risico op een iGAS laag voor huishoudcontacten van patiënten met roodvonk, het relatieve risico op iGAS werd echter meer dan 12 keer vergroot.(7) De kans op het ontwikkelen van iGAS bij huishoudcontacten van patiënten met iGAS wordt beschreven als 229-2011 keer zo hoog in vergelijking met de algemene populatie.(8) Gezien dit verhoogde risico op iGAS en herhaalde infecties van huishoudcontacten wordt internationaal frequent profylactische antibiotica voor huishoudcontacten toegepast.(9)
Op de intensive care van ons ziekenhuis namen we een 47-jarige man (patiënt A) op en enkele dagen later zijn 73-jarige moeder; beiden met respiratoire insufficiëntie op basis van iGAS. De vrouw van patiënt A had keelpijn en één van zijn twee kinderen had koorts; zij zijn 3 dagen behandeld met azitromycine. Iets later werd een 74-jarige vrouw (patiënt C) opgenomen met een pneumonie en STSS op basis van iGAS; haar ex-man is 2 dagen na haar opgenomen op de intensive care met iGAS. Hun kleinkinderen hadden ze recent gezien bij het kerstdiner en hadden op dat moment verschijnselen van een bovenste luchtweginfectie, de kleinkinderen en andere huishoudcontacten werden 3 dagen behandeld met azitromycine.
Bovenstaande casus illustreren duidelijk het verhoogde risico op iGAS bij huishoudcontacten van iGAS patiënten en de noodzaak tot vroegtijdige profylaxe. De laagdrempeligere behandeling van gezins- en huishoudcontacten bij iGAS infecties past onzes inziens in het goed gebruik van antibiotische profylaxe waarbij mortaliteit en morbiditeit kan worden voorkomen in een duidelijk gedefinieerde risicogroep met een veilig, effectief en betaalbaar middel.
Corieke van der Bas, anios intensive care
Marnix Kuindersma, internist-intensivist
dr. Jerome Lo Ten Foe, arts-microbioloog
Gelre ziekenhuizen Apeldoorn
Acuut reumatische koorts
Bij groep-A-streptokokken hoort ook het ziektebeeld acuut reumatische koorts. Een aandoening die we in Nederland nog maar zelden zien (of zelden herkennen?). Daarom heb ik naar aanleiding van dit artikel 2 vragen:
1. klopt het dat het ziektebeeld acuut reumatische koorts tegenwoordig minder voorkomt dan vroeger, en zo ja, wat is hiervoor de verklaring?
2. kunnen we, gezien de stijging van het aantal invasieve infecties met groep-A-streptokokken, ook een toename van acuut reumatische koorts verwachten? Zijn hier data over beschikbaar?